
【题目】下列说法错误的是( )
A. 0.3 molH2SO4 B. 1 molH2O C. 0.5 molNa D. 1.5 mol氧
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在常温常压(或稍低温度)下合成,其熔点-64.5℃,沸点-5.5℃,遇水易水解。实验室模拟制备装置如图所示(部分夹持装置省略),D中三颈烧瓶置于-10℃冰盐水中。
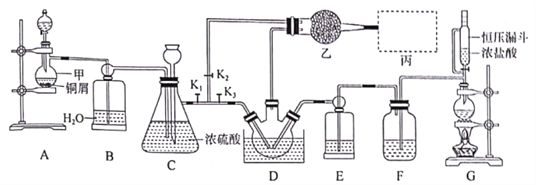
经查阅资料,相关物质性质如下:
①NO2熔点-64.5℃,沸点-5.5℃,可发生反应Cl2+2NO2=2NClO2
②NO与NaOH溶液不反应,但NO2+NO+2NaOH =2NaNO2+H2O
(1)仪器甲的名称是__________。
(2)图示装置中恒压漏斗与分液漏斗相比,其优点为_________________。
(3)NOC1分子中各原子均满足8电子稳定结构,则NOCl的电子式为_________。
(4)实验开始时,先打开K1、K2,关闭K3,打开分液漏斗活塞滴人适量稀硝酸,至C中红棕色完全消失后,关闭K1、K2,此时装置C的作用为_________ ;滴入适量浓盐酸,点燃酒精灯,当______(填装置符号)中充满黄绿色气体时,打开K1、K3,制备NOCl。
(5)装置乙中装有无水CaCl2,其作用为____________;丙为尾气处理装置,则最佳选择为_________。

(6)若实验开始时,先关闭K2,打开K1、K3 ,使NO与Cl2直接反应制备NOC1,会引起什么后果________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A、B、C、D分别为AlCl3、NaOH、NH4HSO4、Na2CO3溶液,实验过程和记录如下图所示(无关物质已经略去):
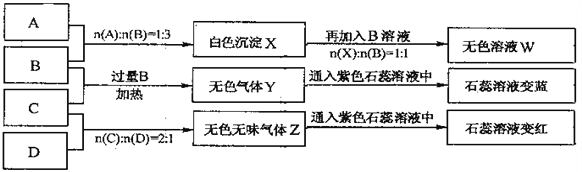
请回答:
(1)W的溶液加热蒸干并灼烧最后所得固体为__________。
(2)D溶液pH___(填“大于”、“小于”或“等于”)7,原因是(用离子方程式表示)_______。
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是_________。(用化学式表示)
(4)等物质的浓度的C溶液与NH4Cl溶液相比较,c(NH4+):前者_____后者(填“<”“>”“=”)。
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中含有的少量杂质,不能用“加入NaOH溶液,分液”的方法除去的是
A.溴苯中的溴B.苯中的苯酚
C.硝基苯中的硝酸D.乙酸乙酯中的乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.3-戊醇和2-甲基-2-丁醇互为同系物
B.顺-2-丁烯和反-2-丁烯的加氢产物不同
C.CH2=C(CH3)2的名称是2-甲基-2-丙烯
D.沸点:1-丁醇>戊烷>2-甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物的成分。

(1)B装置的作用是___________________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有_______气体产生,写出D中发生反应的离子方程式_______。若去掉C,是否能得出同样结论并解释其原因______________。
(3)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3,而不含FeO,请完成表中内容。(试剂,仪器和用品自选)
实验步骤 | 预期现象 | 结论 |
取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解;___________ | ____________________ | 固体残留物仅为Fe2O3 |
(4)若E中收集到的气体只有N2,其物质的量为x mol,固体残留物Fe2O3,的物质的量为y mol,D中沉淀物质的量为z mol,根据氧化还原反应的基本规律,x、y和z应满足的关系为______________。
(5)结合上述实验现象和相关数据的分析,完成硫酸亚铁铵[(NH4)2Fe(SO4)2]在500℃时隔绝空气加热完全分解的化学方程式__________________。
(6)用氧化还原滴定法测定制备得到的TiO2试样中的TiO2的质量分数:在一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵[NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①TiCl4水解生成TiO2·xH2O的化学方程式为_______________。
②滴定终点的现象是_______________。
③滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol·L-1NH4Fe(SO4)2标准溶液20mL,则TiO2的质量分数为_______________。
④若在滴定终点读取滴定管刻度时,俯视标准溶液的液面,使其测定结果_______(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示的四种实验操作名称从左到右依次是( ) 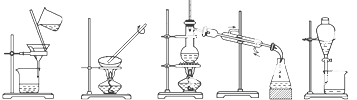
A.过滤、蒸发、蒸馏、分液
B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液
D.分液、蒸馏、蒸发、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备纯硅反应是SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g);ΔH=+QkJ·mol-1(Q>0)。某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是 ( )
Si(s)+4HCl(g);ΔH=+QkJ·mol-1(Q>0)。某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是 ( )
A. 反应过程中,增大压强能加快反应速率,提高SiCl4的转化率
B. 若反应开始时SiCl4为1 mol,则平衡时,吸收热量为QkJ
C. 将反应的温度由T1升高至T2,则反应的平衡常数K1>K2
D. 当反应吸收热量为0.25QkJ时,生成的HCl恰好能与1 molNaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com