
【题目】某温度下,向一定体积0.1 mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则( )
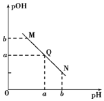
A.N点处pH>pOH,则N点处所示溶液呈酸性
B.该温度下水的离子积Kw=1×10-2a
C.Q点所示溶液呈中性,则M、N、Q三点中只有Q点溶液中水的电离出的c(H+)与水的电离c(OH-)相等
D.M点所示溶液的导电能力强于Q
【答案】B
【解析】
A.如果pOH>pH,则溶液中c(OH-)<c(H+),溶液呈酸性,同理如果pOH=pH,溶液呈中性,如果pOH<pH,则溶液呈碱性,根据图知,所以M、Q、N点溶液分别为酸性、中性、碱性,则N点处所示溶液呈碱性,A错误;
B.水的离子积常数Kw=c(OH-)·c(H+)=(1×10-a)×(1×10-a)=1×10-2a,B正确;
C.任何电解质溶液中都存在水的电离出的c(OH-)=c(H+),与溶液酸碱性无关,所以M、Q、N点溶液中都存在水的电离出的c(H+)与水的电离c(OH-)相等,C错误;
D.电解质溶液导电性强弱与离子浓度成正比,与溶液酸碱性无关,M、Q点溶液中溶质都为醋酸钠和醋酸,但M点醋酸钠浓度小于Q点,所以M点离子浓度小于Q点,所以Q点溶液导电能力强,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】工业上用铝土矿![]() 主要成分为
主要成分为![]() 、
、![]() 、
、![]() 提取氧化铝做冶炼铝的原料,提取的操作流程如下:
提取氧化铝做冶炼铝的原料,提取的操作流程如下:
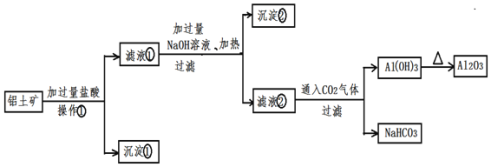
请回答下列问题:
![]() 操作
操作![]() 的名称:______
的名称:______
![]() 沉淀
沉淀![]() 的化学式:______沉淀
的化学式:______沉淀![]() 的化学式:______
的化学式:______
![]() 写出沉淀
写出沉淀![]() 与NaOH溶液反应的化学方程式:______
与NaOH溶液反应的化学方程式:______
![]() 写出滤液
写出滤液![]() 与NaOH溶液反应生成沉淀
与NaOH溶液反应生成沉淀![]() 的离子方程式:______
的离子方程式:______
![]() 尝试写出滤液
尝试写出滤液![]() 中通入
中通入![]() 后的反应方程式:______
后的反应方程式:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生活应用实例中,涉及氧化还原反应的是
A. 用白醋去除水垢
B. 用热的纯碱溶液清洗油污
C. 用风油精(含石蜡油)清洗透明胶残胶
D. 补铁剂(有效成分为Fe2+)与含维生素C共服效果更佳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9~3.8,常温下,酒石酸(用H2T表示)水溶液中三种微粒所占的分数(a)与pH的关系如图所示。下列表述不正确的是( )
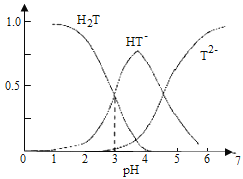
A.葡萄酒中除了存在酒石酸外,还存在酒石酸盐
B.常温下,H2T![]() H++HT-,Ka=10-3
H++HT-,Ka=10-3
C.当葡萄酒的pH为3.7时,HT-所占分数达到最大,此时葡萄酒中H2T>T2-
D.当HT-和T2-物质的量浓度相等时,溶液中水电离出来的氢离子浓度小于纯水中氢离子的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)冬季是雾霾的高发季节,天气预报会及时发布PM2.5的污染警报。
①下列行为不会增加城市大气中PM2.5浓度的是______(填字母)。
a.燃放烟花爆竹 b.为城市主干道洒水保洁 c.露天焚烧落叶
②雾霾会刺激呼吸道,使人易患流行性感冒。感冒发烧病人可服用______(填字母)药品进行治疗。
a.补血剂 b.抗酸药 c.阿司匹林
③维生素C可增强人体的免疫力。维生素C具有的性质是______(填字母)。
a.还原性 b.常温下不溶于水 c.溶液显碱性
(2)著名物理化学家张存浩院士在氟化氢(氘)激光器和水煤气合成液体燃料研究等方面做出了重要贡献。
①氟化氢(HF)的水溶液能腐蚀玻璃。该反应的化学方程式为______,制备普通玻璃的主要原料有SiO2、CaCO3、______(填化学式)。
②水煤气的主要成分是CO和H2,在40 MPa、380 ℃、锌铬氧化物作催化剂的条件下,用CO和H2合成液体燃料CH3OH,该反应的化学方程式为______。
(3)海底考察、水底打捞中均需要进行潜水作业。
①一种简易潜水器是潜水钟,由钢铁制成,在海水中会发生______腐蚀,反应中得到电子的物质是______。
②潜水员需要均衡的膳食结构。糖类、油脂、蛋白质都能为人体提供能量。油脂在人体中发生水解生成甘油和______;蛋白质在酶的作用下水解生成______,而被人体吸收。
③考察活动中会产生大量废水和垃圾。含汞离子废水需要处理后再排放,加入适量的硫化钠溶液能使汞离子变成______(填化学式)沉淀而除去;随便丢弃聚乙烯塑料膜会造成白色污染,聚乙烯的结构简式是______;如图是贴在某垃圾桶上的标志,该标志的含义是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g)
CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g) ![]() 1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正________v逆(填“>”、“=”或“<”)。该温度下反应达到平衡时,CO2的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V L Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为( )
A.![]() mol·L-1B.
mol·L-1B.![]() mol·L-1C.
mol·L-1C.![]() mol·L-1D.
mol·L-1D.![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制作隐形眼镜的材料应该具有亲水性。聚甲基丙烯甲酯![]() 是制作隐形眼镜的材料之一。其合成路线如下:
是制作隐形眼镜的材料之一。其合成路线如下:

完成下列填空:
![]() 写出结构简式:E______;A的一种同分异构体,能与新制氢氧化铜反应______。
写出结构简式:E______;A的一种同分异构体,能与新制氢氧化铜反应______。
![]() 反应
反应![]() 的有机反应类型______。
的有机反应类型______。
![]() 反应
反应![]() 的试剂和反应条件______。
的试剂和反应条件______。
![]() 反应
反应![]() 的化学方程式______。
的化学方程式______。
![]() 聚甲基丙烯酸羟乙酯
聚甲基丙烯酸羟乙酯![]() 也可制作隐形眼镜
也可制作隐形眼镜![]() 结构简式见图
结构简式见图![]() ,用
,用 制作的隐形眼镜比PMMA制作的亲水性好,原因是______。
制作的隐形眼镜比PMMA制作的亲水性好,原因是______。
![]() 佩戴隐形眼镜最好常滴“人工眼泪”以滋润眼球。有一种“人工眼泪”成分是聚乙烯醇
佩戴隐形眼镜最好常滴“人工眼泪”以滋润眼球。有一种“人工眼泪”成分是聚乙烯醇
![]() 已知乙烯醇
已知乙烯醇![]() 不稳定,写出以乙炔为原料
不稳定,写出以乙炔为原料![]() 其他无机原料任选
其他无机原料任选![]() 制取聚乙烯醇的合成路线___________________。
制取聚乙烯醇的合成路线___________________。![]() 合成路线常用的表示方式为:
合成路线常用的表示方式为:![]() 目标产物
目标产物![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
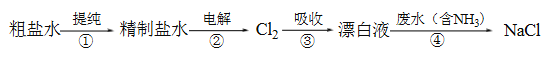
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com