
【题目】某同学在做原电池原理的实验时,有如下实验步骤:
①用导线将灵敏电流计的两端分别与纯净的锌片和铜片相连接(如图1);
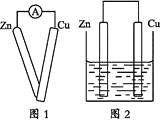
②把一块纯净的锌片插入盛有稀硫酸的烧杯中;
③把一块纯净的铜片插入盛有稀硫酸的烧杯中;
④用导线把锌片和铜片连接起来后,再平行地插入盛有稀硫酸的烧杯中(如图2)。
回答下列问题:
(1)实验步骤①中应观察到的现象是_______________________。
(2)实验步骤②中应观察到的现象是_______________________。
(3)实验步骤③中应观察到的现象是_______________________。
(4)实验步骤④中应观察到的现象是_______________________。
(5)通过实验步骤④该同学头脑中有了一个猜想(或假设),该猜想是_______。
(6)为了证实该猜想,该同学又设计了第⑤步实验,请简要画出第⑤步实验的装置示意图。______
【答案】电流计指针不偏转 锌片上有气泡产生 铜片上无气泡 铜片上有大量气泡,锌片上没有气泡或有少量气泡 有电子从锌经导线向铜片移动 有电子从导线上流过,导线上应形成电流,可以连接一个电流计来证明,实验装置图可设计如下,溶液为稀硫酸。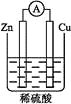
【解析】
形成原电池必须满足下列条件:①两块活泼性不同的金属(或一块金属,一块可导电的非金属)作两极;②电解质溶液;③形成闭合电路;④有自发的氧化还原反应。
(1)没有构成原电池,指针不偏转;
(2)只有锌片,没有构成原电池,锌与稀硫酸直接反应,产生氢气;
(3)只有铜片,没有构成原电池,铜与硫酸不反应,无现象;
(4)构成原电池,锌为负极,逐渐溶解,铜为正极,产生氢气;
(5)构成原电池,外电路有电子(电流)流动;
(6)有电子从导线上流过,导线上应形成电流,可以连接一个电流计来证明,实验装置图可设计如下,溶液为稀硫酸。


科目:高中化学 来源: 题型:
【题目】利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是( )
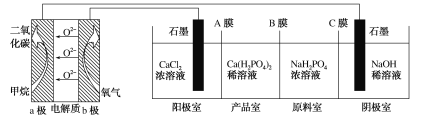
A.a极反应:CH4-8e-+4O2-=CO2+2H2O
B.A膜和C膜均为阴离子交换膜
C.可用铁电极替换阴极的石墨电极
D.a极上通入标况下2.24L甲烷,阳极室Ca2+减少0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组对电解质溶液作如下归纳总结(均在常温下),正确的是( )
①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度均降低
②pH=2的盐酸和pH=1的盐酸,c(H+)之比为2:1
③pH相等的四种溶液:a.CH3COONa;b.NaClO;c.NaHCO3;d.NaOH。其溶液物质的量浓度由小到大顺序为d、b、c、a
④NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)= 2c(SO42-)
⑤已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw;则三者关系为Ka·Kh=Kw
⑥甲、乙两溶液都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙两溶液等体积混合,混合液pH可能等于7
A.①②④B.③④⑥C.④⑤⑥D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃、101 kPa时,反应能量转化关系如图所示,下列说法不正确的是

已知:C(s)+O2(g)===CO2(g) ΔH1;CO(g)+![]() O2(g)===CO2(g) ΔH2;
O2(g)===CO2(g) ΔH2;
A. ΔH2=-282.9kJ·mol-1
B. 2C(s)+O2(g)===2CO(g) ΔH=-221.2 kJ·mol-1
C. ΔH1>ΔH2
D. CO2(g)分解为C(s)和O2(g)是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院深圳研究院成功研发出一种基于二硫化钼/碳纳米复合材料的钠型双离子电池,可充放电。其放电时工作原理如图所示。下列说法不正确的是( )
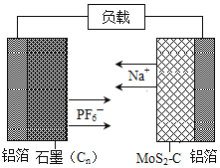
A.二硫化钼/碳纳米复合材料为该电池的负极材料
B.放电时正极的反应式为Cn(PF6)x+xe-═xPF6-+Cn
C.充电时阴极的电极反应式为MoS2-C+xNa++xe-=NaxMoS2-C
D.充电时石墨端铝箔连接外接电源的负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I等)中回收碘,其实验过程如下:
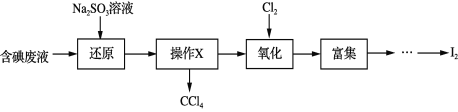
下列叙述不正确的是
A. “操作X”的名称为萃取,可在分液漏斗中进行
B. “还原”步骤发生的反应为:SO32+I2+H2O == 2I+SO42+2H+
C. “氧化”过程中,可用双氧水替代氯气
D. “富集”即I2富集于有机溶剂,同时除去某些杂质离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其中一种理论为厌氧细菌可促使SO42-与H2反应生成S2-,加速钢管的腐蚀,其反应原理如图所示。下列说法正确的是( )

A. 正极的电极反应式为:2H2O+O2+4e-=4OH-
B. SO42-与H2的反应可表示为:4H2+SO42--8e S2-+4H2O
S2-+4H2O
C. 钢管腐蚀的直接产物中含有FeS、Fe(OH)2
D. 在钢管表面镀锌或铜可减缓钢管的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )

A.混合溶液的导电能力与离子浓度和种类有关
B.b点的混合溶液pH=7
C.Na+与A2的导电能力之和大于HA的
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物M的分子式为C9H12,其中可能含有苯环的结构有![]() 、
、 、
、 等,下列说法错误的是
等,下列说法错误的是
A.有机物M不管是否含有苯环,在一定条件下都能发生氧化反应
B.有机物M的一种结构为![]() 该有机物不能与溴单质发生加成反应
该有机物不能与溴单质发生加成反应
C.除了上述三种物质,M的含苯环的同分异构体还有5种(不考虑立体异构)
D.![]() 与苯互为同系物
与苯互为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com