
| AЃЎCl2гыЯЁNaOHШмвКЗДгІЃКCl2+2OHЃЃНClЃ+ClOЃ+ H2O |
| BЃЎFe(OH)3ШмгкЧтЕтЫсЃКFe(OH)3+3H+ЃНFe3++3H2O |
| CЃЎЩеМюШмвКжаМгШыТСЦЌЃКAl + OH- + H2O ЃН AlO2- + H2Ёќ |
| DЃЎBa(OH)2ШмвКжаМгШыЙ§СПAl2(SO4)3ШмвКЃК3Ba2++6OHЃ+2Al3++3SO42ЃЃН3BaSO4Ё§+2Al(OH)3Ё§ |
 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
AЃЎa =3.36ЪБЃЌCO2+2OH- = CO +H2O +H2O |
BЃЎa =4.48ЪБЃЌ2CO2+3OH- = CO +HCO +HCO +H2O +H2O |
CЃЎa =6.72ЪБЃЌCO2+OH- = HCO |
DЃЎa =8.96ЪБЃЌ3CO2+4OH- = CO +2HCO +2HCO +H2O +H2O |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎЩйСПН№ЪєФЦЭЖШыЫЎжаЃКNaЃЋ2H2OЃНNa+ЃЋ2OHЃЃЋH2Ёќ |
| BЃЎ60 mL 1 mol/LДПМюШмвКгы20 mL 2 mol/LЕЈЗЏШмвКЛьКЯЃЈЮоЦјЬхЗХГіЃЉЃК 3CO32-ЃЋ2Cu2+ЃЋ2H2OЃН2HCO3-ЃЋCu2(OH)2CO3Ё§ |
| CЃЎЯђH2OжаЭЖШыЩйСПNa218O2ЙЬЬхЃК2H2OЃЋ2Na218O2ЃН4Na++418OHЃЃЋO2Ёќ |
| DЃЎЯђЬМЫсЧтИЦШмвКжаМгШыЩйСПKOHШмвКЃКCa2+ЃЋ2HCO3-ЃЋ2OH-ЃНCaCO3Ё§ЃЋ2H2OЃЋCO32- |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎзуСПЬњаМШмгкЯЁЯѕЫсЃКFeЃЋ4HЃЋЃЋNO3ЃЃНFe3ЃЋЃЋNOЁќЃЋ2H2O |
| BЃЎСђЛЏФЦШмвКжаЭЈШызуСПСђЛЏЧтЃКH2S + S2ЃЃН2HSЃ |
| CЃЎЬМЫсЧтИЦШмвКжаМгШызуСПЩеМюШмвКЃКHCO3ЃЃЋOHЃЃНCO32ЃЃЋH2O |
DЃЎБНЗгФЦШмвКжаЭЈШыЩйСПЖўбѕЛЏЬМЃК2C6H5OЃЃЋCO2ЃЋH2O  2C6H5OHЃЋCO32Ѓ 2C6H5OHЃЋCO32Ѓ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| БрКХ | ЛЏбЇЗДгІ | РызгЗНГЬЪН | ЦРМл |
| Ђй | СђЫсШмвКжаМгШыBa(OH)2ШмвК | Ba2ЃЋЃЋSO=BaSO4Ё§ | е§ШЗ |
| Ђк | бѕЛЏТСгыNaOHШмвКЗДгІ | 2Al3ЃЋЃЋ3O2ЃЃЋ2OHЃ= 2AlOЃЋH2O | ДэЮѓЃЌAl2O3ВЛгІаДГЩРызгаЮЪН |
| Ђл | ЬњКЭЯЁЯѕЫсЗДгІ | FeЃЋ2HЃЋ===H2ЁќЃЋFe2ЃЋ | е§ШЗ |
| Ђм | ЕШЮяжЪЕФСПЕФFeBr2КЭCl2ЗДгІ | 2Fe2++2Br-+2Cl2=2Fe3++Br2+ 4Cl- | ДэЮѓЃЌРызгЗНГЬЪНжаFe2+гыBr-ЕФЮяжЪЕФСПжЎБШгыЛЏбЇЪНВЛЗћ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎЪЕбщЪвгУДѓРэЪЏКЭЯЁбЮЫсЗДгІжЦШЁЖўбѕЛЏЬМЃК2H++CO32Ѓ==CO2Ёќ+H2O |
| BЃЎЬњКЭЯЁЯѕЫсЗДгІЃКFe+2H+==Fe2++H2Ёќ |
| CЃЎЯђТШЛЏТСШмвКжаМгШыЙ§СПЕФЧтбѕЛЏФЦШмвКЃКAl3++3OHЃ==Al(OH)3Ё§ |
DЃЎгУЧтбѕЛЏФЦМьбщТШЛЏяЇШмвКжаЕФяЇИљРызгЃКNH4++OHЃ NH3Ёќ+H2O NH3Ёќ+H2O |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎгУХЈбЮЫсЫсЛЏЕФKMnO4ШмвКгыH2O2ЗДгІЃЌжЄУїH2O2ОпгаЛЙдадЃК 2MnO  + 6H+ + 5H2O2ЃН 2Mn2+ + 5O2Ёќ + 8H2O + 6H+ + 5H2O2ЃН 2Mn2+ + 5O2Ёќ + 8H2O |
| BЃЎNa2O2гыH2OЗДгІжЦБИO2ЃКNa2O2 + H2OЃН 2Na+ + 2OHЃ + O2Ёќ |
| CЃЎNO2гыЫЎЕФЗДгІЃК3NO2ЃЋH2OЃН2NO3ЃЃЋNOЃЋ2HЃЋ |
DЃЎЯђNaAlO2ШмвКжаЭЈШыЙ§СПCO2ЃК2AlO ЃЋCO2ЃЋ3H2OЃН2Al(OH)3Ё§ЃЋCO2 ЃЋCO2ЃЋ3H2OЃН2Al(OH)3Ё§ЃЋCO2 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
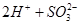 ===
===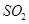 Ёќ
Ёќ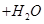 ЕФЛЏбЇЗДгІЪНЙВга
ЕФЛЏбЇЗДгІЪНЙВга| AЃЎ6Иі | BЃЎ8Иі | CЃЎ9Иі | DЃЎ12Иі |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
AЃЎ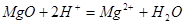 | BЃЎ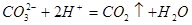 |
CЃЎ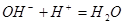 | DЃЎ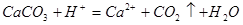 |
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com