
(1)�������Ļ�����Ӧ�ù㷺����FeCl3������������ӡˢ��·ͭ�帯ʴ��������ֹѪ���ȣ�д��FeCl3��Һ��ʴӡˢ��·ͭ������ӷ���ʽ________��
����(1)�еķ�Ӧ��Ƴ�ԭ��أ��뻭��ԭ��ص�װ��ͼ���������������
(2)Ǧ�����dz����Ļ�ѧ��Դ֮һ�����硢�ŵ���ܷ�Ӧ�ǡ�2PbSO4��2H2O![]() Pb��PbO2��2H2SO4
Pb��PbO2��2H2SO4
Ǧ���طŵ�ʱ��________(����������)�ڸ���������Ӧ���ŵ����������Ũ����5 mol/L�½���4 mol/L�����Һ���Ϊ2000 mL(��Ӧ������Һ����仯���Բ���)����ŵ���������·��ת�Ƶ��ӵ����ʵ���Ϊ________mol��
(3)������ƽ�����Pt˿���缫����KOH��Һ�У�Ȼ���������Ϸֱ�ͨ����������������ȼ�ϵ�أ����ȼ�ϵ�ع���ʱ����缫��ӦʽΪ��
������________
������________
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
| �ṩ��ҩƷ��Cl2 ŨH2SO4 NaOH��Һ CuO Cu | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �������Ļ�����Ӧ�ù㷺����FeCl3������ӡˢ��·ͭ�港ʴ��������ֹѪ���ȣ�
�������Ļ�����Ӧ�ù㷺����FeCl3������ӡˢ��·ͭ�港ʴ��������ֹѪ���ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
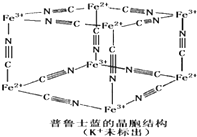 ��1���������Ļ�������������������������Ҫ����;��
��1���������Ļ�������������������������Ҫ����;���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com