
混合物中NaHCO![]() 的质量分数为42%,Na
的质量分数为42%,Na![]() CO
CO![]() 的质量分数为53%,NaCl的质量分数为5%。
的质量分数为53%,NaCl的质量分数为5%。
解析:要计算Na![]() CO
CO![]() 、NaHCO
、NaHCO![]() 和NaCl的质量分数,必求出它们在100 g混合物中各是多少克。从题给条件分析,这三种物质加热只有NaHCO
和NaCl的质量分数,必求出它们在100 g混合物中各是多少克。从题给条件分析,这三种物质加热只有NaHCO![]() 受热分解,而Na
受热分解,而Na![]() CO
CO![]() 、NaCl不分解。加热后剩余残渣为84.5 g,其减少的质量必是NaHCO
、NaCl不分解。加热后剩余残渣为84.5 g,其减少的质量必是NaHCO![]() 加热分解放出去的CO
加热分解放出去的CO![]() 和H
和H![]() O的质量,以此为突破口可求出NaHCO
O的质量,以此为突破口可求出NaHCO![]() 的质量。滴加AgNO
的质量。滴加AgNO![]() 溶液,再加足量稀硝酸,剩余的沉淀12.26 g是AgCl的质量,根据方程式再求出NaCl的质量,最后求出Na
溶液,再加足量稀硝酸,剩余的沉淀12.26 g是AgCl的质量,根据方程式再求出NaCl的质量,最后求出Na![]() CO
CO![]() 的质量。
的质量。
设混合物中含NaHCO![]() 的质量为x,NaCl的质量为y。
的质量为x,NaCl的质量为y。
加热后失去H![]() O和CO
O和CO![]() 的质量为:100 g-84.5 g=15.5 g
的质量为:100 g-84.5 g=15.5 g
2NaHCO3![]() Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑
168 62
X 15.5 g
![]() x=42 g
x=42 g
NaCl+AgNO3==NaNO3+AgCl↓
58.5 143.5
Y 12.26 g
![]() y=5 g
y=5 g
混合物中Na2CO3质量为100 g-42 g-5 g=53 g。


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案科目:高中化学 来源: 题型:
A.NaHCO![]() 和Na
和Na![]() CO
CO![]() B.NaHCO
B.NaHCO![]() 和KHCO
和KHCO![]()
C.KHCO![]() 和K
和K![]() CO
CO![]() D.MgCO
D.MgCO![]() 和KHCO
和KHCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
今有Na![]() CO
CO![]() 、NaHCO
、NaHCO![]() 和NaCl的混合物100 g,加热到质量不再减少为止,其剩余残渣为84.5 g;将残渣溶于水,滴入足量AgNO
和NaCl的混合物100 g,加热到质量不再减少为止,其剩余残渣为84.5 g;将残渣溶于水,滴入足量AgNO![]() 溶液得到白色沉淀,加足量稀硝酸后大部分沉淀消失,剩余沉淀为12.26 g。试计算混合物中Na
溶液得到白色沉淀,加足量稀硝酸后大部分沉淀消失,剩余沉淀为12.26 g。试计算混合物中Na![]() CO
CO![]() 、NaHCO
、NaHCO![]() 和NaCl的质量分数各是多少。
和NaCl的质量分数各是多少。
查看答案和解析>>
科目:高中化学 来源: 题型:
有两种碳酸盐组成的混合物11 g,与足量盐酸充分反应生成CO![]() 4.4 g,该混合物的可能组成是… ( )
4.4 g,该混合物的可能组成是… ( )
A.NaHCO![]() 和Na
和Na![]() CO
CO![]() B.NaHCO
B.NaHCO![]() 和KHCO
和KHCO![]()
C.KHCO![]() 和K
和K![]() CO
CO![]() D.MgCO
D.MgCO![]() 和KHCO
和KHCO![]()
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市东城区(南片)高一上学期期末考试化学试卷(带解析) 题型:填空题
(12分)某课外小组模拟工业流程,设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
(1)分别写出工业上用氨气制取NO及实验室用浓硝酸制取NO 的化学方程式:______________;___________________。
的化学方程式:______________;___________________。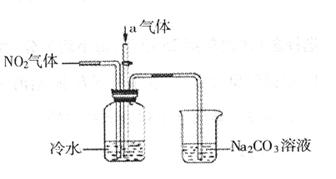
(2)连接好该装置后,首先进行的操作是:_____________________。
(3)通入的气体a是______________(填化学式),通入a的目的是:___________。
(4)盛有Na CO
CO 溶液的烧杯为尾气处理装置,该装置中反应的化学方程式是:
溶液的烧杯为尾气处理装置,该装置中反应的化学方程式是:
_______NO +_______Na
+_______Na CO
CO +_______H
+_______H O=NaNO
O=NaNO +_______+_______NaHCO
+_______+_______NaHCO (完成此方程式)
(完成此方程式)
(5)用N O
O 代替NO
代替NO 与水和a气体反应可生成硝酸,此反应的化学方程式是:
与水和a气体反应可生成硝酸,此反应的化学方程式是:
____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com