
| A、两个反应中还原产物前者为KCl,后者为K2S和N2 |
| B、两个反应均为置换反应 |
| C、若两个反应中生成等物质的量的P2O5和CO2转移电子数之比为5:2 |
| D、火药中的钾盐均作氧化剂 |


科目:高中化学 来源: 题型:
| A、Na、K、Rb |
| B、F、Cl、Br |
| C、Mg2+、Al3+、Zn2+ |
| D、Cl-、Br-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通常把铝粉和氧化铁的混合物叫铝热剂 |
| B、某物质中只含有一种元素,该物质一定是纯净物 |
| C、40K和40Ca的中子数相等、质子数不相等 |
| D、乙烯分子中碳碳双键的键能是乙烷分子中碳碳单键键能的两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
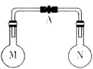 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | H2 | NH3 | NO |
| 气体N | SO2 | Cl2 | HCl | O2 |
| A、①②③④ | B、①④③② |
| C、②④①③ | D、④①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、⑤④①③ | B、⑤①④②③ |
| C、④①②⑤③ | D、③②④①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com