
| A. | 3:2 | B. | 1:6 | C. | 2:3 | D. | 1:1 |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
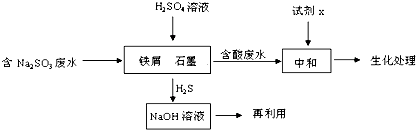
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K、K2O、K2CO3、KHCO3 | B. | Na、Na2O2、NaOH、Na2CO3 | ||
| C. | K、K2O、KOH、K2CO3 | D. | Na、Na2O、NaOH、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 | |
| B. | 用洁净铁丝蘸取两种样品在酒精灯火焰上灼烧,火焰颜色呈黄色的是小苏打 | |
| C. | 分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 | |
| D. | 先将两样品配成溶液,后分别加入石灰水,无白色沉淀生成的是小苏打 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com