解:甲为一种淡黄色固体,且为化合物,应为Na
2O
2,若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成,应为HCl和NH
3的反应,生成NH
4Cl,且A能与O
2反应,应为NH
3,则C为NO,E为NO
2,G为HNO
3,B为H
2O,与Na
2O
2反应生成NaOH,能与NaOH反应的金属为Al,为乙为Al,F为NaAl(OH)
4,则
(1)①反应为NH
3在催化剂条件下发生催化氧化生成NO的反应,反应的化学方程式为4NH
3+5O
2
4NO+6H
2O,
故答案为:4NH
3+5O
2
4NO+6H
2O;
(2)②为Na
2O
2和H
2O的反应,反应的离子方程式为2Na
2O
2+2H
2O═4Na
++4OH
-+O
2↑,③为Al和NaOH的反应,反应的离子方程式为2Al+2OH
-+6H
2O═2[Al(OH)
4]
-+3H
2↑,
故答案为:2Na
2O
2+2H
2O═4Na
++4OH
-+O
2↑,2Al+2OH
-+6H
2O═2[Al(OH)
4]
-+3H
2↑;
(3)反应④为3NO
2+H
2O=2HNO
3+NO,当有3moNO
2l参加反应时,有2mol电子转移,则1molNO
2参加反应,转移的电子的物质的量为

mol,
故答案为:

.
分析:甲为一种淡黄色固体,且为化合物,应为Na
2O
2,若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成,应为HCl和NH
3的反应,生成NH
4Cl,且A能与O
2反应,应为NH
3,则C为NO,E为NO
2,G为HNO
3,B为H
2O,与Na
2O
2反应生成NaOH,能与NaOH反应的金属为Al,为乙为Al,F为NaAl(OH)
4,结合对应物质的性质解答该题.
点评:本题考查无机物的推断,题目难度中等,本题推断的突破口为物质的颜色以及反应现象,学习中注重相关知识的积累.

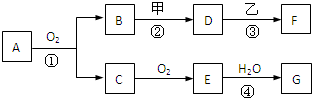 物质的转化关系如图所示,其中甲可由两种单质直接化合得到,乙为金属单质,
物质的转化关系如图所示,其中甲可由两种单质直接化合得到,乙为金属单质, 4NO+6H2O,
4NO+6H2O, 4NO+6H2O;
4NO+6H2O; mol,
mol, .
.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案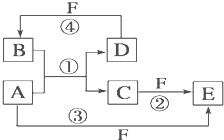 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).

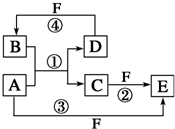 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).

 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平.有关物质的转化关系如图所示:
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平.有关物质的转化关系如图所示: