
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: | B. | NH4Cl的电子式: | ||
| C. | 含78个中子的碘的核素:53131I | D. | 二氧化硅的分子式:SiO2 |
分析 A.氧离子的核电荷数为8,核外电子总数为10;
B.氯离子为阴离子,电子式中氯离子需要标出最外层电子;
C.质量数=质子数+中子数,碘元素的质子数为53,元素符号的左上角为质量数、左下角为质子数;
D.二氧化硫晶体为原子晶体,不存在二氧化硅分子.
解答 解:A.氧离子的核电荷数为8、核外电子总数为10,其正确的离子结构示意图为: ,故A错误;
,故A错误;
B.氯化铵是离子化合物,由氨根离子与氯离子构成,氯离子需要标出所带电荷,其正确的电子式为: ,故B错误;
,故B错误;
C.含78个中子的碘原子的质量数是131,所以78个中子的碘的核素可以表示为:53131I,故C正确;
D.SiO2为二氧化硅的化学式,二氧化硅属于原子晶体,不存在SiO2分子,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及离子结构示意图、元素符号、分子式与化学式、电子式中等知识,明确常见化学用语的概念及书写原则为解答关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 它属于有机高分子 | B. | 它能产生“白色污染” | ||
| C. | 它形成的单体是乙烯 | D. | 聚乙烯中含有双键不稳定,易变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如图:
最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如图: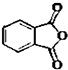 +C4H9OH$\stackrel{H_{2}SO_{4}}{→}$
+C4H9OH$\stackrel{H_{2}SO_{4}}{→}$ 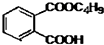 $→_{C_{4}H_{9}OH}^{H_{2}SO_{4}}$
$→_{C_{4}H_{9}OH}^{H_{2}SO_{4}}$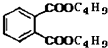
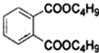 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
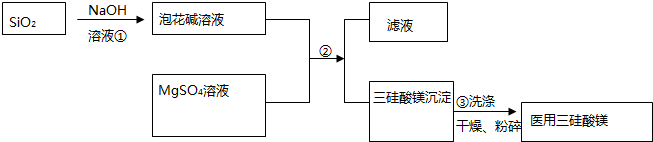
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 天然维生素P(结构如图,)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图,)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A. | 1mol该有机物一定条件下可以和5mol溴水反应 | |
| B. | 该有机物的分子式为C15H8O7R | |
| C. | 1mol该有机物一定条件下最多消耗8 mol H2 | |
| D. | 1mol维生素P可以和4molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 白磷结构如图所示,与O2反应生成P4O6的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则该分子中含有共价键的数目是( )
白磷结构如图所示,与O2反应生成P4O6的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则该分子中含有共价键的数目是( )| A. | 10 | B. | 24 | C. | 12 | D. | 28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某物质的晶体中含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子未画出),晶体中A、B、C的原子个数之比依次为( )
某物质的晶体中含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子未画出),晶体中A、B、C的原子个数之比依次为( )| A. | 1:3:1 | B. | 2:3:1 | C. | 2:2:1 | D. | 1:3:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com