
(10分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10mL2% H2O2溶液 | 无 |
② | 10mL5% H2O2溶液 | 无 |
③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_____________________________________。
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。


分析上图能够得出的实验结论是______________________________________。
(1)降低了活化能(2分)
(2)探究浓度对反应速率的影响 (2分)
向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中)(2分)
(3)2H2O2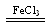 O2↑+2H2O (2分)
O2↑+2H2O (2分)
(4)碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率 (2分)
【解析】
试题分析:(1)催化剂能加快反应速率的原因是能降低反应的活化能。(2)实验①和②,不同的是浓度,所以探究的是浓度对反应速率的影响。由于长时间没有观察到明星现象,说明反应速率很小,可以使用同种同量的催化剂,或同时加热,即将试管放入同一热水浴中。(3)③是过氧化氢在氯化铁做催化剂条件下的反应,故反应写成:2H2O2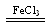 O2↑+2H2O。(4)三个反应中,⑤速率最快,④最慢,说明反应在碱性环境中能增大反应速率,酸性环境能减慢反应速率。
O2↑+2H2O。(4)三个反应中,⑤速率最快,④最慢,说明反应在碱性环境中能增大反应速率,酸性环境能减慢反应速率。
考点:反应速率的影响因素。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:选择题
为配制0.01 mol·L-1的NaCl,下列操作导致所配溶液浓度偏高的是
A.取NaCl样品时不慎在表面沾了点蒸馏水
B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶刻度线
D.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
甲烷燃料电池分别选择H2SO4溶液和NaOH溶液做电解质溶液,下列说法正确的是
A.总反应式都为CH4+2O2===CO2+2H2O
B.H2SO4和NaOH的物质的量都不变,但浓度都减小
C.若用H2SO4溶液做电解质溶液,负极反应式为CH4-4e-+H2O===CO2+4H+
D.若用NaOH溶液做电解质溶液,正极反应式为O2+2H2O+4e-===4OH-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
等质量的四份镁铝合金粉末分别与下列过量的溶液充分反应,放出氢气最多的是
A.NaOH B.稀H2SO4
C.蔗糖 D.NaCl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高一上学期第三次月考化学试卷(解析版) 题型:选择题
在4份碘化钾淀粉溶液中,分别加入下列物质,不能使溶液变蓝的是
A.氯水 B.溴水 C.碘水 D.碘化钠溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列反应中符合下图图像的是
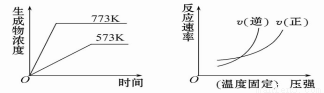
A.N2(g) + 3H2(g)  2NH3(g) ΔH =-Q1 kJ·mol-1 (Q1>0)
2NH3(g) ΔH =-Q1 kJ·mol-1 (Q1>0)
B.2SO3(g)  2SO2(g) + O2(g) ΔH = + Q2 kJ·mol-1 (Q2>0)
2SO2(g) + O2(g) ΔH = + Q2 kJ·mol-1 (Q2>0)
C.4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g) ΔH =-Q3 kJ·mol-1 (Q3>0)
4NO(g) + 6H2O(g) ΔH =-Q3 kJ·mol-1 (Q3>0)
D.H2(g) + CO(g)  C(s) + H2O(g) ΔH = + Q4 kJ·mol-1 (Q4>0)
C(s) + H2O(g) ΔH = + Q4 kJ·mol-1 (Q4>0)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:选择题
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:Zn-2e-+2OH-= Zn(OH)2 Ag2O +H2O + 2e-= 2Ag+2OH-
下列说法正确的是
A.溶液中OH-向正极移动,K+、H+向负极移动
B.锌发生还原反应,氧化银发生氧化反应
C.锌是负极,氧化银是正极
D.在电池放电过程中,负极区溶液碱性增强
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省等四校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列各物质所含原子数目,按由大到小顺序排列的是
①0.6mol NH3 ②标准状况下22.4L He
③4℃ 9mL水(ρ=1g/mL) ④19.6g H2SO4
A.②①③④ B.①③④② C.①④③② D.②③④①
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:选择题
用短线“-”表示共用电子对,用“‥”表示未成键孤对电子的式子叫路易斯结构式。以下路易斯结构式表示的分子属极性分子的是
①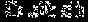 ②.
②.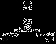 ③.
③. ④.
④.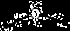
A.①②③④ B.①②③ C.②③④ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com