
【题目】Be(OH)2是两性的,跟强酸反应时生成Be2+,跟强碱反应时生成BeO22—。现有三份等物质的量浓度、等体积的BeCl2、MgCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液,分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mL)的关系如下图所示,则与BeCl2、MgCl2、AlCl3三种溶液对应的图像正确的是
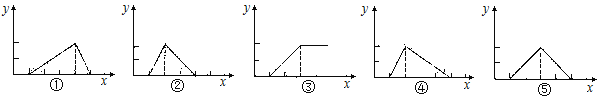
A.③②① B.②③④ C.③⑤④ D.⑤③①
【答案】D
【解析】
试题分析:向氯化镁溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化镁,当氢氧化钠过量时,沉淀也不会溶解,量保持不变,故对应的是图象③,向BeCl2溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化锌,当氢氧化钠过量时,沉淀会溶解,依次发生反应BeCl2+2NaOH=Be(OH)2↓+2NaCl,Be(OH)2+2NaOH=Na2 BeO2+2H2O,沉淀量达到最大和沉淀完全消失所消耗的氢氧化钠是相等的,故图象⑤是正确的,向氯化铝溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化铝,当氢氧化钠过量时,沉淀会溶解,依次发生反应:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3↓+NaOH=NaAlO2+2H2O,沉淀量达到最大和沉淀完全消失所消耗的氢氧化钠的物质的量之比是3:1,故图象①是正确的,故D正确。


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
【题目】我国从1994年起推出加碘食盐工程,目前“加碘盐”主要是在食盐中加入 。在酸性条件下,碘化钾与其反应可生成碘单质,写出该反应的离子方式: 。若用盐酸酸化的碘化钾淀粉溶液检验碘盐中的含碘物质,可观察到的明显现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g) + H2(g) ![]() 2HI(g) △H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:
2HI(g) △H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示:

(1)达平衡时,I2(g)的物质的量浓度为mol/L 。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是 ,则乙条件可能是 。(填入下列条件的序号)
①恒容条件下,升高温度;②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积;④恒温条件下,扩大反应容器体积;⑤恒温恒容条件下,加入正催化剂。
(3)若保持温度不变,在另一个相同的2L密闭容器中加入2mol I2(g)、4mol H2(g)发生反应,达平衡时,HI的体积分数是 0.6(填大于、等于、小于)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明淀粉在酶作用下只部分发生了水解的实验试剂是 ( )
A.碘水 B.氢氧化钠溶液、银氨溶液
C.烧碱溶液、新制Cu(OH)2溶液 D.碘水、烧碱溶液、Cu(OH)2悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5 mol/L盐酸10 mL稀释到200 mL,再取出5 mL,这5 mL溶液的物质的量浓度是
A.0.05 mol/L B.0.25 mol/L
C.0.1 mol/L D.0.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对不同时期原子结构模型的提出时间由早到晚排列正确的是( )
①电子分层排布模型 ②“葡萄干布丁”模型 ③电子云模型
④道尔顿原子学说 ⑤核式模型
A. ④②⑤①③ B. ④②③①⑤
C. ①③②⑤④ D. ④⑤②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.1 L 1 mol L—1硫酸溶液中所含的氧原子数为4NA
B.标准状况下,11.2 L CC14中所含的原子数为2.5NA
C.2.7 g A1与足量氧气充分反应,转移的电子数为0.3NA
D.常温常压下,14 g由N2与CO组成的混合气体中所含的原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
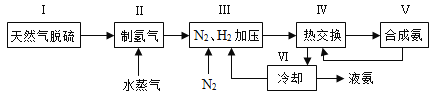
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:____________________。
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g)ΔH=+206.4kJ·mol-1
CO(g)+3H2(g)ΔH=+206.4kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g)ΔH=-41.2kJ·mol-1
CO2(g)+H2(g)ΔH=-41.2kJ·mol-1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是 __。
利用反应②,将CO进一步转化,可提高H2的产量。若1 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为____________。
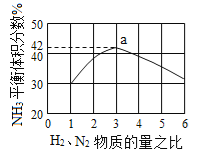
(3)图(a)表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)_____________。简述本流程中提高合成氨原料总转化率的方法:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com