
下列叙述正确的是
A. Fe分别与氯气和稀盐酸反应所得氯化物相同
B.K、Zn分别与不足量的稀硫酸反应所得溶液均呈中性
C. Li、Na、K的原子半价和密度随原子序数的增加而增大
D.C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在下列所示的微粒中,氧化性最强的是( )
|
| A. | 1S22S22P2 | B. | 1S22S22P5 | C. | 1S22S22P63S1 | D. | 1S22S22P6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
阿斯巴甜作为强烈甜味剂被广泛应用于食品、饮料、糖果等,
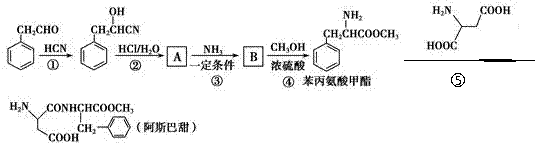 工业上可以用苯丙氨酸甲酯和α-氨基丁二酸为原料合成:
工业上可以用苯丙氨酸甲酯和α-氨基丁二酸为原料合成:
已知:RCN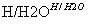 RCOOH;
RCOOH;

 。
。
(1)A中含氧官能团的名称为________________;α-氨基丁二酸的分子式为 。
(2)①、⑤的反应类型依次为 。
(3)B的同分异构体中同时符合下列条件的有2种,写出其结构简式:________________、_______________。
①有三种化学环境不同的氢原子;②含苯环的中性物质。
(4)写出阿斯巴甜与足量NaOH水溶液充分反应的化学方程式:__________________________________。
(5)写出以1,3-丙二醇(HOCH2—CH2—CH2OH)为原料制备 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
CH2===CH2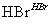 CH3CH2Br
CH3CH2Br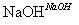 CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
如图中是可逆反应X2+3Y2⇌2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
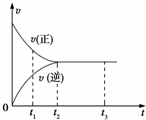
|
| A. | t1时,只有正方向反应 |
|
| B. | t1~t2,X2的物质的量越来越多 |
|
| C. | t2~t3,反应不再发生 |
|
| D. | t2~t3,各物质的浓度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
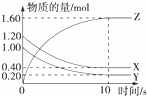
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
①反应的化学方程式为 ;
②0~10s内,用Z表示的化学反应速率 ;
③X的转化率为 ;(转化率是指平衡时某物质反应的物质的量与起始物质的量的百分比)
(2)在一定温度下,可逆反应A(g)+3B(g)⇌2C(g)达到平衡的标志是
A.A的生成速率与C分解的速率相等
B.单位时间内生成nmolA,同时生3nmolB
C.A、B、C的浓度不再变化
D.A、B、C的分子数比为1:3:2.
查看答案和解析>>
科目:高中化学 来源: 题型:
图中X、Y、Z为单质,其他为化学物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
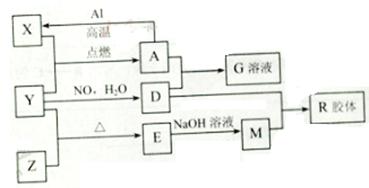
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型为 ;R的化学式是 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为 。
(3)已知A与1molAl反应转化为X时(所有物质均为固体)。放出aKJ热量。写出该反应的热化学方程式:
。
(4)写出A和D的稀溶液反应生成G的离子方程式:
(5)向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。
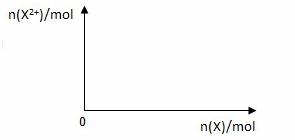
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.01mol下列物质分别加入100mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
①Na2O1 ②Na2O ③Na2CO3 ④NaCl
A.①>②>③>④ B.①>②>④>③
C.①=②>③>④ D.①=②>③=④
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应。X的原子结构示意图为________。
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为__________________________。
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与H2O2反应,其产物之一是Y的单质,Y单质的电子式为____________;Z分子的结构呈____________。
②A的化学式是________________________。
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工业生产中所用的α—Fe催化剂的主要成分是FeO、Fe2O3
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4∶5,其中Fe2+与Fe3+物质的量之比为___________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为_____________(用小数表示,保留2位小数)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
2Fe2O3+C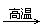 4FeO+CO2↑。为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为_________g。
4FeO+CO2↑。为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com