
(12分)已知反应:①SO3+H2O===H2SO4、②3NO2+H2O===2HNO3+NO
③2F2+2H2O===4HF+O2、④2Na+2H2O===2NaOH+H2↑、
⑤Na2O+2HCl===2NaCl+H2O、⑥SiO2+2NaOH===Na2SiO3+H2O
(1)上述反应中不属于氧化还原反应的有______________________ (填序号,下同).
H2O被氧化的是______,H2O被还原的是______.属于氧化还原反应,但其中的H2O既不被氧化又不被还原的是__________________.
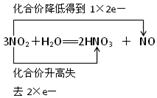
(2) 用双线桥分析反应②:______________________________________________.
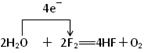
(3) 用单线桥标出反应③的电子转移方向和数目_________________________.
(4)写出反应④的离子方程式:______________________________________________.
(12分)
(1)①⑤⑥ (填序号,下同). ③、 ④、 ②.
(2)
 (3)
(3)
(4) 2Na+2H2O===2Na++2OH-+H2↑
解析试题分析:(1)根据方程式可知,①⑤⑥中元素的化合价都没有变化,不是氧化还原反应。而在反应②中,氮元素的化合价部分升高到+5价,部分降低到+2价,因此NO2既是氧化剂,也是还原剂,而水既不是氧化剂,也不是还原剂;反应③F元素的化合价从0价降低到-1价,单质氟是氧化剂。而水中氧元素的化合价从-2价升高到0价,失去电子,作还原剂;反应④中,钠元素的化合价从0价升高到+1价,失去电子。水中氢元素的化合价从+1价降低到0价,导电得到电子,作氧化剂。
(2)双线桥法:表示同种元素的原子在反应前后转移电子的情况,箭头从反应物指向产物,但并不表示电子转移的方向,桥两端连接同种元素,因此应该表示为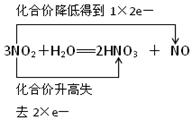 。
。
(3)单线桥中箭头从还原剂中失电子的元素指向氧化剂得电子的元素,由于箭头的方向已经指明电子转移的方向,所以不需要注明得失,但必须注明电子转移的数目。即应该表示为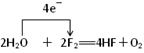 。
。
(4)根据化学方程式可知,该反应的离子方程式是2Na+2H2O===2Na++2OH-+H2↑。
考点:考查氧化还原反应的应该判断和表示方法及离子方程式的书写等。
点评:凡是有元素化合价升降的反应都是氧化还原反应,没有元素化合价升降的反应是非氧化还原反应,所以判断氧化还原反应的关键是准确判断元素的化合价变化。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
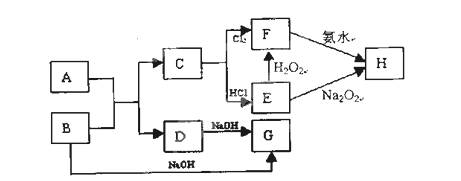
(每空2分,共12分)已知金属氧化物A和金属单质B在高温条件下反应生成C和D的同时放出大量的热;将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色液体。
(1)红褐色液体中H粒子的直径大小范围 。
(2)写出D、E的化学式:D 、E
(3)写出E的酸性溶液与双氧水反应的离子方程式 。
(4)写出F溶液中阳离子的检验方法: 离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(每空2分,共12分)已知金属氧化物A和金属单质B在高温条件下反应生成C和D的同时放出大量的热;将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色液体。
(1)红褐色液体中H粒子的直径大小范围 。
(2)写出D、E的化学式:D 、E
(3)写出E的酸性溶液与双氧水反应的离子方程式 。
(4)写出F溶液中阳离子的检验方法: 离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2011-2012年江西省高一上学期期中考试化学试卷 题型:填空题
(12分)(1)已知离子反应: +6I—+6H+=R—+3I2+3H2O,n= ,R元素在
+6I—+6H+=R—+3I2+3H2O,n= ,R元素在 中的化合价是 。
中的化合价是 。
(2)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:

① 在上述有编号的步骤中,需用氧化剂的是 (填编号)。
②完成并配平下列反应的化学方程式,按要求标出电子转移的方向和数目,并回答问题:
__Na2Cr2O7+__KI+__HCl——__CrCl3+_NaCl+__KCl+__I2+ (用单线桥表示电子转移的方向、数目)
(用单线桥表示电子转移的方向、数目)
当反应中有3mol电子转移时,氧化产物的质量是 。
查看答案和解析>>
科目:高中化学 来源:2013届福建省高二上学期期中考试化学(文)试卷 题型:填空题
(每空2分,共12分)已知金属氧化物A和金属单质B在高温条件下反应生成C和D的同时放出大量的热;将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色液体。
(1)红褐色液体中H粒子的直径大小范围 。
(2)写出D、E的化学式:D 、E
(3)写出E的酸性溶液与双氧水反应的离子方程式 。
(4)写出F溶液中阳离子的检验方法: 离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年深圳高级中学高二下学期期末测试化学 题型:选择题
( 12 分)已知:

甲苯及其卤代物是有机化工的基本原料,由它出发可制造某些香料、药物及广泛应用于
印刷、电子工业中的感光树脂的重要中间体,它们之间的关系如下图所示:
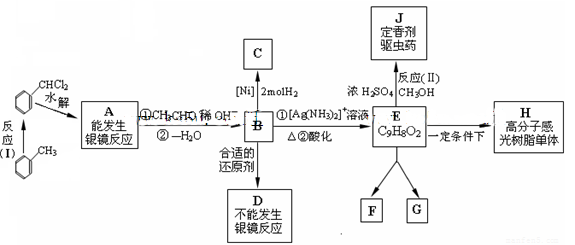
图中B、D、E都能使溴水褪色,E在光等辐射能作用下可以发生二聚加成反应,生成互为同分异构体的环状化合物F和G;E还可以在一定条件下形成一种优质高分子感光树脂的单体H。试回答:
⑴写出有机物的结构简式:A____________、C_____________、D_____________。
⑵反应(I)的类型是______________,反应(II)的类型是______________。
⑶完成化学方程式:A→B:____________________________________________。
⑷写出高分子感光树脂单体H的结构简式______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com