
【题目】连二亚硫酸钠(Na2S2O4)又称保险粉,是白色砂状或淡黄色粉末固体,己知连二业硫酸钠在碱性条件下较稳定,易被空气氧化,不溶于甲醇,遇水迅速分解,某同学设计利用如下图所示的实验装置制备一定量的连二亚硫酸钠,装置C中的试剂为甲酸钠(HCOONa)、NaOH 的甲醇溶液,回答下列问题:
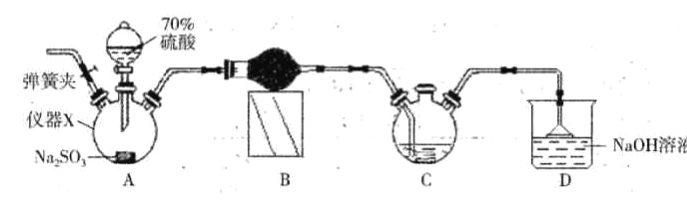
(1)仪器X的名称是_____。装置B中的球形干燥管中盛装的试剂是_______。
(2)装置D的作用是___________。实验时需要将C中温度控制在70-75℃,最好的控制方法是__________。
(3)实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是______。实验过程中装置C 中除有气体产生外,还能观察到的实验现象为____________。
(4)有同学通过仔细思考后认为,还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是______。为得到较纯的连二亚硫酸钠,需要对在过滤时得到的连二亚硫酸钠进行洗涤,洗涤的方法是_________。
(5)若实验中所用Na2SO3的质量为12.6g (硫酸是过量的),最终得到m g干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为_____________。
【答案】 三颈烧瓶 无水CaCl2或P2O5 吸收过量的SO2,防止其污染空气 水浴加热 排出装置中的O2,避免其氧化连二亚硫酸钠 有(白色或淡黄色)固体生成 吸收水蒸气 在无氧环境中,向漏斗中加入甲醇至浸没晶体,待甲醇顺利流下后,重复2-3次 m/8.7×100%
【解析】(1)根据构造可判断仪器X的名称是三颈烧瓶。装置B用来干燥二氧化硫,二氧化硫是酸性氧化物,因此其中的球形干燥管中盛装的试剂是无水CaCl2或P2O5。(2)二氧化硫属于大气污染物,装置D的作用是吸收过量的SO2,防止其污染空气。实验时需要将C中温度控制在70~75℃,最好的控制方法是水浴加热。(3)连二亚硫酸钠易被空气氧化,装置中含有空气,因此实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是排出装置中的O2,避免其氧化连二亚硫酸钠。由于连二亚硫酸钠是白色砂状或淡黄色粉末固体,因此实验过程中装置C 中除有气体产生外,还能观察到的实验现象为有白色或淡黄色固体生成。(4)由于D装置中的水蒸气有可能进入到C装置中,因此还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是吸收水蒸气。由于产品易被氧化,不溶于甲醇,遇水迅速分解,所以洗涤的方法是在无氧环境中,向漏斗中加入甲醇至浸没晶体,待甲醇顺利流下后,重复2~3次。(5)Na2SO3的质量为12.6g,物质的量是0.1mol,根据S原子守恒可知理论上得到产品质量是0.05mol×174g/mol=8.7g,最终得到mg干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为m/8.7×100%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】100mL2mol/L的硫酸和过量的锌片反应,为了加快反应速率,但又不影响生成氢气的总量,不宜采取的措施是
A. 改用锌粉 B. 升温反应体系的温度
C. 加入少量的CuSO4溶液 D. 改用200mLlmol/L的硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙酸是弱酸的实验事实是
A. CH3COOH溶液与Zn反应放出H2
B. 0.1 mol/L CH3COONa溶液的pH大于7
C. CH3COOH溶液与NaCO3反应生成CO2
D. 0.1 mol/L CH3COOH溶液可使紫色石蕊变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积固定为2L的密闭容器中进行下列反应。
(1)将1 mol N2O4放入此容器,N2O4发生如下反应:N2O4(g)![]() 2NO2(g)(正反应吸热),平衡时,测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍,此时N2O4的体积分数为Φ。平衡时容器内NO2和N2O4的物质的量之比为______________;升高温度,N2O4的转化率______________(增大或减小);
2NO2(g)(正反应吸热),平衡时,测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍,此时N2O4的体积分数为Φ。平衡时容器内NO2和N2O4的物质的量之比为______________;升高温度,N2O4的转化率______________(增大或减小);
(2) 恒温时,向此容器内加入1 mol NO2,发生如下反应:2NO2(g)![]() N2O4(g)。达到平衡时,其它条件不变,若向容器中分别增加①1 mol NO2或②1 mol N2O4,重新达到平衡后,与第一次平衡时相比,NO2的体积分数______________。
N2O4(g)。达到平衡时,其它条件不变,若向容器中分别增加①1 mol NO2或②1 mol N2O4,重新达到平衡后,与第一次平衡时相比,NO2的体积分数______________。
A. ①②都增大 B. ①②都减小 C. ①增大,②减小 D. ②增大,①减小
(3) 恒温时,向此容器内加入x mol NO2 和y mol N2O4(y≥0),若要使平衡后N2O4的体积分数仍为Φ,且反应朝着逆反应方向进行,则x的取值范围是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列反应不能制得括号中纯净物质的是
A. 乙烯与氯气加成(1,2 二氯乙烷)
B. 氯气与苯用氯化铁作催化剂反应(氯苯)
C. 等物质的量的氯气与乙烷在光照条件下反应(氯乙烷)
D. 乙烯与水加成(乙醇)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工作者把烃的通式用键数的形式表示,给研究有机物分子中键能大小的规律带来了很大的方便。设键数用I表示,则烷烃中碳原子数与键数的关系通式为CnI3n+1,那么饱和一元醇中碳原子数跟键数关系的通式应为( )
A.CnI3n-1B.CnI3n+1C.CnI3n-2D.CnI3n+2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化

下列说法正确的是
A. 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ
B. 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量
C. 通常情况下,N2(g)和O2(g)混合能直接生成NO
D. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示构成细胞的元素和化合物的图解,a、b、c、d代表不同的小分子物质,A、B、C代表不同的大分子物质,请分析回答下列问题:

(1)物质A、B、C、d共有的元素有______________ 。
(2)物质b的结构通式为___________________,其分子结构的特点是_______________________。
(3)物质C在植物叶肉细胞中分布于_____________ 、 _____________ 和线粒体。
(4)若物质A在动物、植物细胞中均可含有,并且作为细胞内最理想的储能物质,不仅含能量多而且体积较小,则A是______。物质d是______,胆固醇与图中物质 _______(填字母)、维生素D都属于固醇类物质。
(5)物质B的多样性决定于b的_________________________________以及自身的空间结构。若物质B由n个b形成的一条多肽链(直链物质),则B中至多含有________个肽键,至少含有________个氮原子,至少含有________个氧原子; 叶肉细胞的细胞质中b有________种。
(6)将染色体的成分C提取出来,彻底水解后的产物是_________种。细胞中的RNA与C相比特有的是_______________________________________________(答案要全面)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com