
分析 (1)该反应中Fe元素化合价由+3价变为+6价,Cl元素化合价由0价变为-1价;
(2)失电子化合价升高的元素被氧化,得电子化合价降低的反应物是氧化剂;
(3)根据氯气和转移电子之间的关系式计算消耗氯气体积;
(4)胶体微粒直径在10-9m~10-7m或1 nm~100nm之间.
解答 解:(1)该反应中Fe元素化合价由+3价变为+6价,Cl元素化合价由0价变为-1价,转移电子总数为6,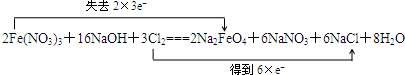 ,
,
故答案为: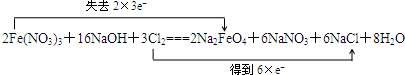 ;
;
(2)该反应中Fe元素化合价由+3价变为+6价,Cl元素化合价由0价变为-1价,该反应中Fe元素化合价升高被氧化,Cl2是氧化剂,故答案为:铁;Cl2;
(3)设消耗氯气气体体积为x,
2Fe(NO3)3+16NaOH+3Cl2=2Na2FeO4+6NaNO3+6NaCl+8H2O转移电子
67.2L 6×6.02×1023
x 2.408×1024
67.2L:6×6.02×1023=x:2.408×1024
x=$\frac{2.408×1{0}^{24}×67.2L}{6×6.02×1{0}^{23}}$=44.8L,
故答案为:44.8L;
(4)胶体微粒直径在10-9m~10-7m或1 nm~100nm之间,胶体能产生丁达尔效应,故答案为:10-9m~10-7m或1 nm~100nm.
点评 本题考查氧化还原反应,涉及氧化还原反应计算、基本概念等知识点,明确各个物理量之间关系即可解答,知道常见元素化合价.


科目:高中化学 来源: 题型:解答题
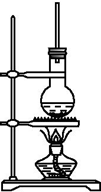 如图为硬脂酸甘油酯在碱性条件下水解的装置图.进行皂化反应时的步骤如下:
如图为硬脂酸甘油酯在碱性条件下水解的装置图.进行皂化反应时的步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化学与生活:防治环境污染,改善生态环境已成为全球的共识.
化学与生活:防治环境污染,改善生态环境已成为全球的共识.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1 | B. | △H2 | C. | △H3 | D. | △H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cl2溶于水 | |
| B. | NH3溶于水 | |
| C. | 可充电电池的反应如H2O+Zn+Ag2O$?_{充电}^{放电}$Zn(OH)2+Ag | |
| D. | 电解水生产H2和O2,点燃H2和O2的混合物生产水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物可能含共价键 | |
| B. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| C. | 离子化合物中只含离子键 | |
| D. | 离子化合物中一定含有金属离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 温度/℃ | 25 | 170 | 230 | 400 | 450 | 700 |
| 质量/g | 1.00 | 0.88 | 0.76 | 0.76 | 0.27 | 0.27 |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com