
| A. | NH4H是离子化合物 | |
| B. | NH4H溶于水,所形成的溶液显酸性 | |
| C. | NH4H与水反应时,NH4H是还原剂 | |
| D. | NH4H固体投入少量的水中,有两种气体生成 |
分析 A、依据题意NH4H与化铵的结构相似,则性质也应相似,氯化铵是铵盐属于离子化合物,因此NH4H也是离子化合物,由NH4+和H-构成的;
B、题中给出了NH4H与水反应有H2生成可知,NH4H与水发生了氧化还原反应,标注化合价看出,是NH4H中负一价氢阴离子与水中正一价的氢元素间发生的氧化还原反应,NH4H做还原剂,水做氧化剂,产物为NH3•H20和H2,所得溶液呈碱性;
C、NH4H与水发生了氧化还原反应,标注化合价看出,是NH4H中负一价氢阴离子与水中正一价的氢元素间发生的氧化还原反应,NH4H做还原剂,水做氧化剂;
D、NH4H固体投入少量的水中,由于发生的氧化还原反应是放热的,生成的NH3•H20分解为NH3和H20,所以可以得到两种气体.
解答 解:A、NH4H与氯化铵的结构相似,是由NH4+和H-构成的离子化合物,故A正确;
B、NH4H与水发生了氧化还原反应,NH4H+H20=NH3•H20+H2↑,生成的NH3•H20是弱碱水溶液中呈碱性,故B错误;
C、根据NH4H和H20反应过程中化合价的升降,可知NH4H中H-化合价升高为0价,做还原剂,故C正确;
D、NH4H与水发生反应时放热,生成的NH3•H20分解,NH3•H20$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H20,所以生成了两种气体,故D正确;
故选B.
点评 本题考查了铵盐的结构、一水合氨的性质及氧化还原反应的基本原理和信息应用能力,重点考查化合价标注和氧化还原反应的判断.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:解答题
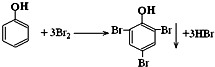
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
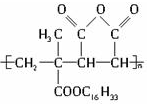 下列有关J的说法正确的是( )
下列有关J的说法正确的是( )| A. | J是由2种单体缩聚而成的 | B. | J是由2种单体加聚而成的 | ||
| C. | J具有可燃性 | D. | J没有可燃性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCH3+(碳正离子)中含有电子数为10NA | |
| B. | 1mol铜与足量硫蒸气反应,转移电子数为2NA | |
| C. | 用惰性电极电解CuCl2溶液,阴极析出32g铜时,线路中通过的电子数为NA | |
| D. | 0.84g NaHCO3晶体中阳离子和阴离子总数为0.03NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 氧化剂 | 还原剂 | 其它反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | FeCl3 | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
| ③ | KClO3 | HCl(浓) | Cl2 | Cl2 | |
| ④ | KMnO4 | HCl(浓) | Cl2 | MnCl2 |
| A. | 第①组反应的氧化产物一定只有FeCl3(实为Fe3+) | |
| B. | 第③组反应的产物还有KCl和H2O | |
| C. | 氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+ | |
| D. | 还原性比较:H2O2>Mn2+>Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com