
已知A、B、C、D都是短周期元素,它们的原子半径大小为B>C>D>A。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。回答下列问题(用元素符号或化学式表示)。
(1)M分子中B原子轨道的杂化类型为 。
(2)化合物CA3的沸点比化合物BA4的高,其主要原因是 。
(3)写出与BD2互为等电子体的C3-的结构式 。
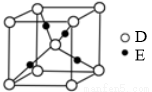
(4)E+的核外电子排布式为 ,下图是D、E形成的某种化合物的晶胞结构示意图,该晶体1个晶胞中阳离子的个数为 。
(5)向E的硫酸盐溶液中通入过量的CA3,可生成[E(CA3)4]2+配离子,1 mol [E(CA3)4]2+中含有σ键的数目为 。
(1)sp2 (2)NH3分子间能形成氢键 (3)[N=N=N]-
(4)1s22s22p63s23p63d10 4
(5)16mol(或16×6.02×1023)
【解析】
试题分析:根据题意知,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,则B为碳元素;D原子有2个未成对电子,A、B、D三种元素组成的一种化合物M为甲醛,原子半径大小为B>C>D>A,则A为氢元素,D为氧元素,C为氮元素; E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,则E为铜元素。(1)甲醛的结构式为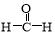 ,分子中碳元素原子轨道的杂化类型为sp2;(2)化合物NH3的沸点比化合物CH4的高,其主要原因是NH3分子间能形成氢键;(3)与CO2互为等电子体的N3-的结构式为[N=N=N]-;(4)铜为29号元素,Cu+的核外电子排布式为1s22s22p63s23p63d10,根据O、Cu形成的某种化合物的晶胞结构示意图利用分摊法确定,该晶体1个晶胞中阳离子的个数为8×1/8+1=2;(5)向硫酸铜溶液中通入过量的NH3,可生成[Cu (NH3)4]2+配离子,在[Cu(NH3)4]2+中四个NH3通过配位键与Cu2+结合,在每个NH3中含有3个共价键,所以在阳离子[Cu(NH3)4]2+中含有的共价键为3×4+4=16.因此1mol该配合物中含有σ键的数目为16mol(或16×6.02×1023)。
,分子中碳元素原子轨道的杂化类型为sp2;(2)化合物NH3的沸点比化合物CH4的高,其主要原因是NH3分子间能形成氢键;(3)与CO2互为等电子体的N3-的结构式为[N=N=N]-;(4)铜为29号元素,Cu+的核外电子排布式为1s22s22p63s23p63d10,根据O、Cu形成的某种化合物的晶胞结构示意图利用分摊法确定,该晶体1个晶胞中阳离子的个数为8×1/8+1=2;(5)向硫酸铜溶液中通入过量的NH3,可生成[Cu (NH3)4]2+配离子,在[Cu(NH3)4]2+中四个NH3通过配位键与Cu2+结合,在每个NH3中含有3个共价键,所以在阳离子[Cu(NH3)4]2+中含有的共价键为3×4+4=16.因此1mol该配合物中含有σ键的数目为16mol(或16×6.02×1023)。
考点:考查物质结构与性质。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、硫酸型酸雨的形成会涉及反应:2H2SO3+O2
| ||||
| B、明矾放入水中可形成带正电的Al(OH)3胶粒:Al3++3H2O?Al(OH)3(胶体)+3H+ | ||||
| C、选用CuSO4溶液除去乙炔气体中的H2S:H2S+Cu2+═CuS↓+2H+ | ||||
| D、热的纯碱液可以清洗油污的原因:CO32?+2H2O?H2CO3+2OH? |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市毕业班调研测试理综化学试卷(解析版) 题型:填空题
(16分)(1)乙醇是重要的有机化工原料,可由乙烯直接水合法生产。
已知:甲醇脱水反应①2CH3OH(g) = CH3OCH3(g)+H2O(g)?△H1=-23.9KJ·mol-1
甲醇制烯烃反应②2CH3OH(g) = C2H4 (g)+2H2O(g)?△H2=-29.1KJ·mol-1
乙醇异构化反应③CH3CH2OH(g) = CH3OCH3(g))? △H3=+50.7KJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g) C2H5OH(g) △H= ;
C2H5OH(g) △H= ;
(2)乙烯气相直接水合反应,在其他条件相同时,分别测得C2H4的平衡转化率在不同压强(P1、P2)下随温度变化的曲线如下图。结合曲线归纳平衡转化率-T曲线变化规律:
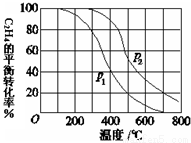
(a) ;
(b) ;
(3)若要进一步提高乙烯的转化率,可以采取的措施有 。
A.增大乙烯的浓度 B.分离出乙醇 C.加催化剂
(4)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。
①t℃时,反应达到平衡时n(CO):n(CO2)= 。
②若在1 L密闭容器中加入0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时FeO(s)转化率为50%,求x的值。(写出计算步骤)
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
在0.5 L溶液中含有0.1 mol NaCl和0.2 mol MgCl2,则此溶液中氯离子的物质的量浓度是
A、0.3 mol·L-1 B、0.5 mol·L-1
C、0.6 mol·L-1 D、1 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
标准状况下,112 mL某气体的质量是0.17g,该气体可能是
A、O2 B、N2 C、H2S D、CO2
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:填空题
某铝土矿中主要含有Al2O3、Al(OH)3、AlO(OH),还含有Fe2O3等杂质。利用拜耳法生产氧化铝的流程如下图所示:

(1)碱浸时为提高铝土矿的浸出率可采取的措施是 , 。(答两点)
(2)AlO(OH)与NaOH反应的化学方程式为 。
(3)在稀释、结晶过程中,加Al(OH)3晶核的目的是促进Al(OH)3的析出。上述“稀释、结晶”工艺,也可用通入足量的某气体的方法来代替。通入气体时发生反应的离子方程式是 .
(4)浓缩所得的NaOH溶液由于吸收了空气中的CO2而含有杂质,该杂质可通过苛化反应除去,写出苛化反应的化学方程式: 。
(5)该生产流程能实现 (填化学式)的循环利用。
(6)氧化铝是工业上冶炼铝的原料,用氧化铝电解制备金属铝时需加入冰晶石(Na3AlF6)作助熔剂,写出用NaF和Al2(SO4)3反应制备冰晶石的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海 水为电解质溶液,示意图如下。
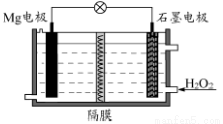
该电池工作时,下列说法不正确的是
A.Mg电极是该电池的负极
B.H2O2在石墨电极上发生还原反应
C.石墨电极附近溶液的pH增大
D.溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源:2015届江苏省、常州一中、沭阳中学高三联合调研化学试卷(解析版) 题型:选择题
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol·L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是

A.图中A点对应溶液的pH:a=1
B.生成沉淀的最大质量m=2.33g
C.原混合液中盐酸物质的量浓度为0.1mol·L-1
D.当V[Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2+ + SO42- BaSO4↓
BaSO4↓
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三质量调研化学试卷(解析版) 题型:选择题
铁氧体(Fe3O4)法是处理含铬废水的常用方法,其原理是:用FeSO4把废水中Cr2O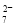 还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物(
还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3·FeO)的复合氧化物(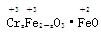 )。处理含1 mol Cr2O
)。处理含1 mol Cr2O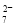 废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
废水至少需要加入a mol FeSO4·7H2O。下列结论正确的是
A.x=0.5,a=10 B.x=1,a=5 C.x=2,a=10 D.x=0.5,a=8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com