
右图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 A.工业上合成X的氢化物采用高温高压催化剂条件
A.工业上合成X的氢化物采用高温高压催化剂条件
B.Z2水溶液中通入YO2后褪色,表现了YO2的漂白性
C.常压下五种元素的单质中,Z单质的熔点最高
D.Y、Z的阴离子电子层结构都与R原子的相同
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
下列有关阿伏伽德罗常数说法正确的是
A.含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA
B.标况下,22.4L四氯化碳所含分子数大于NA
C.0.1mol/L 的AgNO3溶液中,阳离子所带正电荷数目为0.1NA
D. 0.2mol/L的 H2SO4的硫酸溶液与0.1mol/L的 H2SO4的硫酸溶液等质量混合溶液浓度大于0.15mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.1mol有机化合物A与标准状况下5.6L氧气混合,一定条件下两者完全反应,只有CO、CO2和H2O三种产物,将全部产物依次通入足量的浓硫酸和碱石灰中,浓硫酸增重5.4克,碱石灰增重4.4克,还有标准状况下2.24L气体的剩余,求:
(1)有机化合物A的分子式(要求写出推理过程);
(2)若有机化合物A能与钠反应放出氢气,请写出A的结构简式;
(3)写出所有比A多一个—CH2—原子团的同系物的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为蕃茄电池(注:番茄汁中含有苹果酸、柠檬酸等有机酸),下列说法正确的是( )
A.一段时间后,锌片质量会变小
B.铜电极附近会出现蓝色
C.电子由铜通过导线流向锌
D.锌电极是该电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下, 将 3 mol SO2 和 1 mol O2 充入一定容密闭容器中, 在催化剂存在下进行下列反应: 2SO2(g) + O2(g)  2SO3(g); 当达到平衡状态时, 下列说法中正确的是( )
2SO3(g); 当达到平衡状态时, 下列说法中正确的是( )
A.生成 SO3 为2 mol B.SO2 和 SO3 物质的量之和一定为 3 mol
C.消耗SO2 的速率等于生成O2的速率 D.SO2 的物质的量和SO3 物质的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水提取溴的过程中,吸收塔内溴蒸气和吸收剂SO2发生的化学反应为:
Br2 + SO2 + 2H2O = 2HBr + H2SO4 ,下列说法正确的是( )
A.Br2在反应中表现还原性 B.1mol氧化剂在反应中得到2mol电子
C.Br2在反应中失去电子 D.SO2在反应中被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中两种气体的分子数一定相等的是
A.温度相同、体积相同的O2和N2 B.质量相等、密度不等的N2和C2H4
C.体积相同、密度不等的CO和C2H4 D.压强相同、体积相同的O2和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有NH4+、Ba2+、Mg2+、Ag+、OH-、SO42-、CO32- 中的某几种,现用该溶液做以下实验:①取此溶液少许,加入足量盐酸无明显现象;②另取少许加入足量浓氢氧化钠溶液,有白色沉淀生成;③将②中沉淀过滤,取滤液微热,有无色刺激性气味气体放出,该气体能使湿润的红色石蕊试纸变蓝。
由此推断,该溶液中肯定有 离子,肯定没有 离子。
写出②中发生反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。

Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s)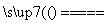 Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________。检验是否存在该杂质的方法是____________________________。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:________________________________________________________________________
________________________________________________________________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O +I2===S4O
+I2===S4O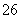 +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
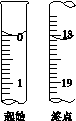
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为____________________________________________。
,常用作脱氯剂,该反应的离子方程式为____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com