

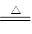 K2CO3+CO2↑+H2O(3分)
K2CO3+CO2↑+H2O(3分)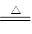 K2CO3+H2O+CO2↑,故答案为:2KHCO3
K2CO3+H2O+CO2↑,故答案为:2KHCO3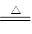 K2CO3+H2O+CO2↑;
K2CO3+H2O+CO2↑;

 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,为了防止事故,使用前可用于检验氯仿是否变质
,为了防止事故,使用前可用于检验氯仿是否变质| A.淀粉一碘化钾溶液 | B.NaOH溶液 | C.酚酞溶液 | D.硝酸酸化的AgNO3溶液 |
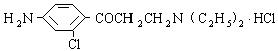 ,它可以以甲苯为原料合成
,它可以以甲苯为原料合成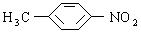 ,其反应方程式为______________________________________,再经过________________反应(填反应类型)来合成
,其反应方程式为______________________________________,再经过________________反应(填反应类型)来合成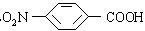 ,再经过一系列反应来合成。
,再经过一系列反应来合成。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
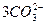 ====
====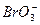 +5Br-+3CO2↑;③
+5Br-+3CO2↑;③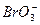 + 5Br-+6H+====3Br2+3H2O。其中反应②中的氧化剂是_________________;还原剂是_________________。
+ 5Br-+6H+====3Br2+3H2O。其中反应②中的氧化剂是_________________;还原剂是_________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
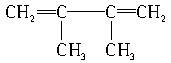 和y mol CH2==CH—CN经加聚形成高聚物A,A在适量的氧气中完全燃烧生成二氧化碳、水蒸气和氮气,其中二氧化碳占总体积的52.6%,则x∶y约是( )
和y mol CH2==CH—CN经加聚形成高聚物A,A在适量的氧气中完全燃烧生成二氧化碳、水蒸气和氮气,其中二氧化碳占总体积的52.6%,则x∶y约是( )| A.1∶1 | B.1∶2 | C.2∶3 | D.3∶2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
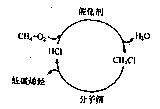
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②①③④ | B.①②③④ | C.③②①④ | D.②①④③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com