
 ��Դ����������������ٵ��ش���⣬�״���δ����Ҫ����Դ����֮һ��
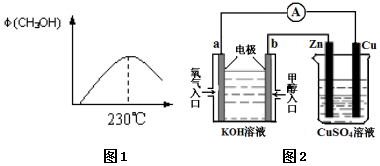
��Դ����������������ٵ��ش���⣬�״���δ����Ҫ����Դ����֮һ������ ��1��230�洦��ƽ��״̬���������¶ȼ״������������˵�������¶�ƽ�����淴Ӧ�����ƶ���
��2��˵�������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��
��3���μӷ�ӦCOΪ2.5mol��90%=2.25mol����������ƽ��ʱ������������ʵ��������º����£�ѹǿ֮�ȵ������ʵ���֮�ȣ�
��4���ټ״�ȼ�ϵ�أ�ȼ���ڸ�������������Ӧ��bΪ������b�缫�ϼ״�ʧȥ���ӣ���������������̼���������ˮ���ɵ缫����ʽ�ж�PH�仯��
�ڸ��ݵ���ת���غ������������������������ܷ�Ӧ����ʽ�жϣ�
��5�����ݸ�˹���������㷴Ӧ���ʱ䲢��д�Ȼ�ѧ����ʽ���¶ȣ�Ũ�ȵȶ����ʵ�ת������Ӱ�죮
��� �⣺��1��230�洦��ƽ��״̬���������¶ȼ״������������˵�������¶�ƽ�����淴Ӧ�����ƶ����������¶�ƽ�������ȷ�Ӧ�ƶ���������ӦΪ���ȷ�Ӧ�����H��0���ʴ�Ϊ������
��2������ӦΪ���ȷ�Ӧ�������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С����K��1���ʴ�Ϊ������
��3���μӷ�ӦCOΪ2.5mol��90%=2.25mol����
CO��g��+2H2��g��?CH3OH��g�� �������ʵ�����С
1 2
2.25mol 4.5mol
��ƽ��������������ʵ���Ϊ2.5mol+7.5mol-4.5mol=5.5mol�����º����£�ѹǿ֮�ȵ������ʵ���֮�ȣ���ʱ�����ڵ�ѹǿΪ��ʼʱ��$\frac{5.5mol}{2.5mol+7.5mol}$=0.55����
�ʴ�Ϊ��0.55��
��4���ټ״�ȼ�ϵ�أ�ȼ���ڸ�������������Ӧ����bΪ������b�缫�ϼ״�ʧȥ���ӣ���������������̼���������ˮ���缫��ӦʽΪ��CH3OH+8OH--6e-=CO32-+
6H2O���ɵ缫��Ӧ����ʽ֪OH-���ϼ�С����PH��С�������ڷ�����Ӧ�����ӷ�ʽΪ��Zn+Cu2+=Zn2++Cu��
�ʴ�Ϊ������CH3OH+8OH--6e-=CO32-+6H2O����С��Zn+Cu2+=Zn2++Cu��
�ڵ�ͭƬ�������仯Ϊ12.8gʱ�����ĵ�n��Cu��=$\frac{12.8}{64}$=0.2mol����Cu��Cu2+ת�Ƶĵ�����Ϊ2mol����n��e-��=0.4mol�����ݵ���ת���غ��֪��������Ϊ$\frac{0.2mol��2}{4}$=0.1mol����a�������ĵ�O2�ڱ�״���µ����Ϊ0.1mol��22.4L/mol=2.24L��Zn+CuSO4=Cu+ZnSO4��CuSO4���ϵ����ĵ�����������������С��
�ʴ�Ϊ��0.4mol��2.24����С��
��5����2CO2��g��+2H2O��l���TC2H4��g��+3O2��g����H1=+1411.0kJ/mol
��2CO2��g��+3H2O��l���TC2H5OH��1��+3O2��g����H2=+1366.8kJ/mol
���ݸ�˹���ɷ�ӦC2H4��g��+H2O��l���TC2H5OH��l�����ڢ�-�٣����ԡ�H=��H2-��H1=-44.2 kJ/mol����ΪC2H4��g��+H2O��l���TC2H5OH����H=-44.2 kJ/mol��
�����¶�����ȷ�����У��ʽ����¶ȿ������ϩת���ʣ����ϵ������������Ӧ��Ũ�����ӣ��ʷ�Ӧ������Ӧ�������Ҳ�������ϩת���ʣ�
�ʴ�Ϊ��C2H4��g��+H2O��l���TC2H5OH����H=-44.2kJ/mol�������¶ȣ����ϵ������Ҵ���
���� ���⿼�黯ѧƽ�������Ӱ�����ء�ƽ�ⳣ����ԭ�������ԭ���ȣ��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
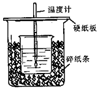 ��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 672 mL | B�� | 168 mL | C�� | 504 mL | D�� | 224 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 Ϊ̽���ⶨ�к��ȵ�ʵ�飬С������50mL 0.50mol•L-1������50mL 0.55mol•L-1NaOH��Һ������ͼ��ʾ��װ���н����кͷ�Ӧ����ͨ���ⶨ��Ӧ���������ų��������������к��ȣ��к�����ֵΪ57.3kJ/mol����
Ϊ̽���ⶨ�к��ȵ�ʵ�飬С������50mL 0.50mol•L-1������50mL 0.55mol•L-1NaOH��Һ������ͼ��ʾ��װ���н����кͷ�Ӧ����ͨ���ⶨ��Ӧ���������ų��������������к��ȣ��к�����ֵΪ57.3kJ/mol�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ȫ���ܽ�ʱ���μӷ�Ӧ����������ʵ���һ����0.4 mol | |
| B�� | �μӷ�Ӧ�Ľ����������� 3.6 g��m��9.6 g | |
| C�� | �����ɵij������ﵽ���ʱ������NaOH��Һ�����V=200 mL | |
| D�� | ������ȫ���ܽ�ʱ�ռ���NO���������ڱ����Ϊ 2.24 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
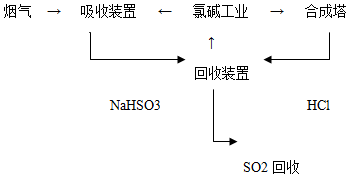
| �����Ʋ� | ʵ�鲽�輰���� |
| �ף�������Fe��OH��3���� �ң����������ϣ����ܷ�����Ӧ�� Fe3++6SO2?Fe��SO2��63+����Ӧb�� | I���Ʊ�Fe��OH��3���岢���� II���ֱ���Fe��OH��3����ú��ɫҺ���м����������ۣ���ǰ�߲���ɫ�����߱�Ϊdz��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ú�Ϳ���ʯ�ͷ����ã�������ȼ�Ϻͱ������������� | |
| B�� | ʯ���ǻ���������Ʒ����Ϊ������ | |
| C�� | ú������Ҫ�õ���̿��ú���͡��ְ�ˮ�ͽ�¯�� | |
| D�� | ʯ�ͷ���ɻ�����ᡢ������������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com