
| A. | ①②③④ | B. | ③②①④ | C. | ②③①④ | D. | ②①③④ |
分析 根据N=nNA知,分子数与物质的量成正比,物质的量越大其分子数越多,根据n=$\frac{m}{M}$结合分子构成计算物质的物质的量,据此分析解答.
解答 解:所含原子的物质的量为4mol的H2,每个分子中含有2个H原子,所以n(H2)=$\frac{1}{2}$n(H)=$\frac{1}{2}$×4mol=2mol;
n(H2O)=$\frac{45g}{18g/mol}$=2.5mol;
n(O2)=$\frac{16g}{32g/mol}$=0.5mol,
据N=nNA知,分子数与物质的量成正比,物质的量越大其分子数越多,
所以物质的量从多到少顺序是③②①④,则分子数从多到少顺序是③②①④,
故选B.
点评 本题考查物质的量的有关计算,为高频考点,明确物质的量个数中各个物理量的关系及分子构成即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
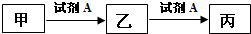
| A. | 若A为硝酸,X为金属元素,则甲与丙反应可生成乙 | |
| B. | 若乙为NaHCO3,则丙一定是CO2 | |
| C. | 若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质 | |
| D. | 若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量稀盐酸 | B. | 加入适量稀硫酸 | ||
| C. | 加入适量烧碱固体 | D. | 加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和反应是放热反应 | |
| B. |  H2燃烧时的能量变化如图所示 | |
| C. | 化学键断裂放出能量 | |
| D. | 反应物总能量与生成物总能量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
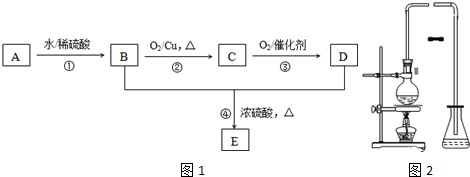
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
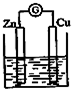 X,Y,Z,W为按原子序数由小到大排列的四种短周期的元素,X的阳离子为质子,Y原子有3个能级,各能级电子数相等,Z,W位于同一周期,Z是该周期中金属性最强的元素,W的单质是黑火药的重要成分,含有该单质的某种膏药可治疗某些皮肤病.请回答下列问题:
X,Y,Z,W为按原子序数由小到大排列的四种短周期的元素,X的阳离子为质子,Y原子有3个能级,各能级电子数相等,Z,W位于同一周期,Z是该周期中金属性最强的元素,W的单质是黑火药的重要成分,含有该单质的某种膏药可治疗某些皮肤病.请回答下列问题: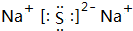 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
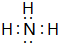 ,空间结构为三角锥形.
,空间结构为三角锥形.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com