
 下图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去).已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀.
下图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去).已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀. .
.分析 F是地壳中含量最多的金属元素的单质,则F为Al;转化关系中X电解得到三种物质,为电解电解质与水型,A、B为气态单质,二者为氢气和氯气,二者反应生成D,D为HCl,E为黑色固体,为氧化物,和HCl反应又生成B气体,A为H2,B为Cl2,E为MnO2,电解X是电解氯化钠溶液,所以X为NaCl,C为NaOH,与Al反应生成G,G为NaAlO2;M为红褐色沉淀为Fe(OH)3,所以J是含三价铁离子的物质,是H和D反应生成,证明J为FeCl3,H、I为氧化物判断H为Fe2O3,I为红棕色气体为NO2,结合转化故选可知,N为HNO3,Y为Fe(NO3)3,结合物质的性质来解答.
解答 解:F是地壳中含量最多的金属元素的单质,则F为Al;转化关系中X电解得到三种物质,为电解电解质与水型,A、B为气态单质,二者为氢气和氯气,二者反应生成D,D为HCl,E为黑色固体,为氧化物,和HCl反应又生成B气体,A为H2,B为Cl2,E为MnO2,电解X是电解氯化钠溶液,所以X为NaCl,C为NaOH,与Al反应生成G,G为NaAlO2;M为红褐色沉淀为Fe(OH)3,所以J是含三价铁离子的物质,是H和D反应生成,证明J为FeCl3,H、I为氧化物判断H为Fe2O3,I为红棕色气体为NO2,结合转化故选可知,N为HNO3,Y为Fe(NO3)3,
(1)B为Cl2中所含元素位于周期表第三周期第ⅦA族,故答案为:第三周期第ⅦA族;
(2)X为NaCl,NaCl的电子式为 ,
,
故答案为: ;
;
(3)J为FeCl3,检验J中阴离子即氯离子的常用试剂是HNO3、AgNO3,故答案为:HNO3、AgNO3;
(4)G(NaAlO2)+J(FeCl3)→M(Fe(OH)3)的反应是在水溶液中发生的双水解反应,反应离子方程式是:3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓,
故答案为:3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓;
(5)依据分析推断可知Y为Fe(NO3)3,受热分解生成二氧化氮和氧化铁,依据原子守恒配平书写的化学方程式是:4Fe(NO3)3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+12NO2↑+3O2↑,
故答案为:4Fe(NO3)3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+12NO2↑+3O2↑.
点评 本题考查了物质转化关系和物质性质的应用,主要考查离子方程式的书写、盐类水解的应用等,物质颜色与反应特点是解题关键,对学生的分析思维能力有较高的要求,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| B. | 稀醋酸与0.1 mol•L-1 NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热△H=-110.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成元素相同,组成元素的质量分数也对应相等的不同化合物,一定互为同分异构体 | |
| B. | 组成元素相同,相对分子质量相同的几种化合物,互为同分异构体 | |
| C. | 摩尔质量相同,各元素质量分数也对应相等的不同化合物,一定是同分异构体 | |
| D. | 凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制饭勺、高压锅等的不锈钢是纯铁 | B. | 铝制品可以长期用作餐具 | ||
| C. | Al(OH)3可用于制胃酸中和剂 | D. | 医用酒精浓度是95% |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
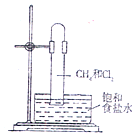 取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )
取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )| A. | 此反应无光照也可发生 | |
| B. | 甲烷和Cl2反应后的产物只有CH3Cl和HCl | |
| C. | 盛放饱和食盐水的水槽底部会有少量晶体析出 | |
| D. | CH4和Cl2完全反应后液面上升,液体充满试管 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com