
某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积百分数。
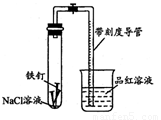
(1)实验前用碱液清洗铁钉,再用0.100mol/L的H2SO4溶液浸泡至有气泡产生。用H2SO4溶液浸泡的目的是_____ 。
(2)为尽量减小误差,下列操作的正确顺序是______ (填序号)。
①装人铁钉②插入注射器向铁钉表面滴入适量 NaCl溶液并打开止水夹③将导管口浸入品红溶液④塞 上单孔活塞⑤检查装置气密性
(3)实验中试管内发生的总反应为__ ____ ;用该实验方案测量空气中O2的体积百分数时应测量的数据是:①导管与试管内部空间总体积,②___ ___ 。
(4) 实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析,请补充 写出假设三:
假设一:电解质溶液的PH不同
假设二: NaCl溶液的浓度不同
假设三:
(5)借助上述实验装置,通过调节溶液的pH验证假设一,获得了如下实验数据:

①当pH=2时,没有观察到稳定液柱形成的原因是__ ____
②根据实验数据分析,为缩短实验测定时间,pH的最佳范围是______
③按上述实验装置,设计实验证明假设二。
第一步:___________ ;
第二步::相同温度下,加入系统表面积的铁钉,组装两套完全相同的上述装置,分别用注射器将NaCl溶液滴入铁钉表面;
第三步:记录形成稳定液柱所用时间和液柱的高度,比较分析数据得出结论。
(1)除去铁钉表面的铁锈;
(2)⑤①④②③
(3)4Fe+3O2+6H2O=4Fe(OH)3;吸入导管内的品红溶液;
(4)铁钉的表面积(温度、催化剂)
(5)①溶液的酸性太强,铁容易发生析氢腐蚀;
②6.0<PH≤6.5
③配置不同浓度的NaCl溶液;
【解析】
试题分析:(1) 铁钉表面由铁锈,可以用稀硫酸除去。(2) 试验装置装药品之前首先要检验气密性,(3) 氯化钠溶液显中性,铁钉在中性溶液中和氧气发生吸氧腐蚀,总反应为:4Fe+3O2+6H2O=4Fe(OH)3;随着反应的进行,试管内氧气减少,压强降低,在大气压的作用下,烧杯中的品红溶液进入带刻度导管,反应掉的氧气等于导管内的品红溶液的体积(4) 实验时发现上述测量过程因反应较慢耗时较长,说明反应速率慢,回答问题时应该从影响化学反应速率的因素方面答题;(5)①当pH=2时,溶液显酸性,铁钉发生析氢腐蚀,产生气体,液柱为0;②当PH的范围为:6.0<PH≤6.5反应的时间最短,产生的液柱最高。③假设二为NaCl溶液的浓度不同,首先要配置不同浓度的NaCl溶液。
考点: 钢铁腐蚀 影响化学反应速率的因素


 阅读快车系列答案
阅读快车系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com