
徐光宪在《分子共和国》一书中介绍了许多明星分子,如H2O2、CO2、BF3、CH3COOH等.下列说法正确的是( )
A.H2O2分子的空间构型为直线形
B.CO2分子为非极性分子
C.BF3分子中的B原子满足8电子稳定结构
D.CH3COOH分子中C原子均为sp2杂化
科目:高中化学 来源:2015-2016学年山东省潍坊市高一下学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.Cu→CuO→Cu(OH)2每步转化均能通过一步反应实现
B.铝合金是一种混合物,它比纯铝的熔点高
C.金属铜放置在潮湿的空气中会被锈蚀,生成绿色的铜锈——碱式碳酸铜
D.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下学期期中考试化学试卷(解析版) 题型:选择题
已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是( )
A.碳的燃烧热为△H = -110.5 kJ/mol
B.1molC(s)所具有的能量一定高于1molCO(g)所具有的能量
C.稀硫酸与稀NaOH溶液反应的中和热为△H = -57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,也放出57.3 kJ 热量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期期中考试化学试卷(解析版) 题型:填空题
黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物。室温为非活性物质。温度升高后变得活泼。在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:

回答下列问题:
(1)在FeS2中的S2-的核外电子排布式是________________________;
(2)常温下Fe3+比Fe2+要更加稳定的原因是__________________________________;
(3)将FeS2与稀盐酸反应得到H2S2,H2S2分子中,共价键的类型是___________________;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是______________________ ,写出两个与SO2互为等电子体的分子或离子_______________________。-
(4)H2SO4和H2SO3都是S的含氧酸,请用结构知识解释H2SO4比H2SO3酸性强的原因:
_____________________________________________________________________。
(5)FeS2的晶体中的Fe2+离子的排列方式如下图。
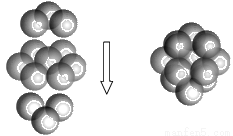
①每个Fe2+周围最近的等距离的S22-离子有____________个。
②已知FeS2的晶胞参数是a0=0.54nm,它的密度为_____________________g·cm-3(列式并计算,阿伏加德罗常数为6.02×1023)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期期中考试化学试卷(解析版) 题型:选择题
根据键能数据估算CH4(g)+4F2(g)═CF4(g)+4HF(g)的反应热△H为( )
化学键 C﹣H C﹣F H﹣F F﹣F
键能/(kJ/mol) 414 489 565 155
A.﹣1940 kJ/mol B.+1940 kJ/mol C.﹣485 kJ/mol D.+485 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期期中考试化学试卷(解析版) 题型:选择题
已知次氯酸分子的结构式为H﹣O﹣Cl,下列有关说法正确的是( )
A.依据其结构判断该含氧酸为强酸
B.O原子与H、Cl都形成σ键
C.该分子为直线形非极性分子
D.该分子的电子式是H:O:Cl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省十三校高一下学期期中考试化学试卷(解析版) 题型:填空题
为清理路面积雪人们使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)X元素在元素周期表中的位置,该融雪剂的化学式是________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是________;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,电子式为________。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中加热时生成的产物的电子式为________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省十三校高一下学期期中考试化学试卷(解析版) 题型:选择题
下列关于化学键的说法正确的是( )
①含有金属元素的化合物一定是离子化合物 ②第IA族和第ⅦA族原子化合时,一定生成离子键 ③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键 ⑤离子键就是阴、阳离子间的相互引力 ⑥含有离子键的化合物一定是离子化合物 ⑦离子化合物中可能同时含有离子键和共价键
A.①②⑤ B.④⑥⑦ C.①④③ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宝应县高一下学期期中调研联合考试化学试卷(解析版) 题型:选择题
一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2  2NH3(正反应是放热反应)。下列有关说法正确的是
2NH3(正反应是放热反应)。下列有关说法正确的是
A.达到化学反应限度时,可生成2mol NH3
B.向容器中再加入N2,可以加快反应速率
C.降低温度可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com