
【题目】在四个不同的容器中,在不同的条件下进行合成氨反应:N2(g)+3H2(g)![]() 2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
A.v(H2)=0.2mol·L-1·min-1
B.v(N2)=0.2 mol·L-1·min-1
C.v(N2)=0.02 mol·L-1·s-1
D.v(H2)= 0.04 mol·L-1·s-1
【答案】C
【解析】
试题分析:都用氮气的浓度变化表示化学反应速率,并且单位一致,然后再进行比较。A.v(H2)=0.2mol·L-1·min-1,则v(N2)=1/3 v(H2)=0.067 mol·L-1·min-1 ;B.v(N2)=0.2 mol·L-1·min-1;C.v(N2)=0.02 mol·L-1·s-1,用mol·L-1·min-1表示速率单位是v(N2)=1.2 mol·L-1·min-1;D.v(H2)= 0.04 mol·L-1·s-1,用mol·L-1·min-1表示速率单位,则v(N2)= (0.04×60)÷3=0.8 mol·L-1·min-1,可见产生氨气速率最快的是选项C。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
A.NH4H是离子化合物,含有离子键和共价键
B.NH4H与水反应时,NH4H是还原剂
C.NH4H投入少量的水中,有两种气体产生
D.NH4H溶于水,所形成的溶液成酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH![]() CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
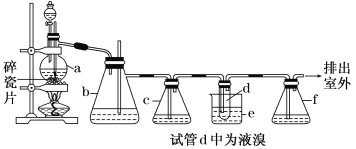
有关数据列表如下:
乙醇 | 1,2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入________(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是______________________。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________(填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________(填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是______________________; 但不用冰水进行过度冷却,原因_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是生活生产中常见的物质,表中列出了它们的(主要)成分
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
名称 | 酒 精 | 醋酸 | 火碱 | 食盐 | 铜线 | 氨气 | 苏打 | 小苏打 |
主要成分 | CH3CH2OH | CH3COOH | NaOH | NaCl | Cu | NH3 | Na2CO3 | NaHCO3 |
根据情景回答问题
(1)请你对表中①~的主要成分进行分类:属于电解质的是____________(填编号)
(2)写出⑧的主要成分溶于水的电离方程式_______________________________
(3)写出NaHCO3受热分解的化学方程式_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有效去除大气中的NOx,保护臭氧层,是环境保护的重要课题。
(1)在没有NOx催化时,O3的分解可分为以下两步反应进行;
①O3=O+O2 (慢) ②O+O3=2O2 (快)
第一步的速率方程为v1=k1c(O3),第二步的速率方程为v2=k2c(O3)·c(O)。其中O为活性氧原子,它在第一步慢反应中生成,然后又很快的在第二步反应中消耗,因此,我们可以认为活性氧原子变化的速率为零。请用k1、k2组成的代数式表示c(O)=____________。
(2)NO做催化剂可以加速臭氧反应,其反应过程如图所示:
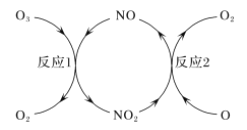
已知:O3(g)+O(g)=2O2(g) ΔH=-143 kJ/mol
反应1:O3(g)+NO(g)=NO2(g)+O2(g) ΔH1=-200.2 kJ/mol。
反应2:热化学方程式为____________________________。
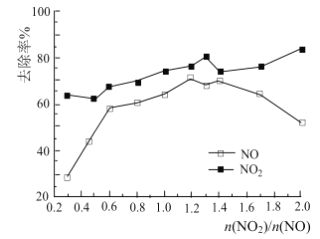
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变![]() ,NOx的去除率如图所示。
,NOx的去除率如图所示。
已知:NO与Ca(OH)2不反应;
NOx的去除率=1-![]() ×100%
×100%
①![]() 在0.3-0.5之间,NO吸收时发生的主要反应的离子方程式为:___________。
在0.3-0.5之间,NO吸收时发生的主要反应的离子方程式为:___________。
②当![]() 大于1.4时,NO2去除率升高,但NO去除率却降低。其可能的原因是__________。
大于1.4时,NO2去除率升高,但NO去除率却降低。其可能的原因是__________。
(4)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-759.8 kJ/mol,反应达到平衡时,N2的体积分数随![]() 的变化曲线如图。
的变化曲线如图。
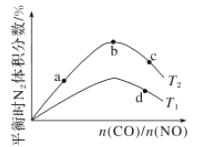
①b点时,平衡体系中C、N原子个数之比接近________。
②a、b、c三点CO的转化率从小到大的顺序为________;b、c、d三点的平衡常数从大到小的顺序为__________(以上两空均用a、b、c、d表示)。
③若![]() =0.8,反应达平衡时,N2的体积分数为20%,则NO的转化率为_____。
=0.8,反应达平衡时,N2的体积分数为20%,则NO的转化率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-VOCl2电池是一种基于阴离子传导的新型二次电池,其简化装置示意图如下。总反应为Mg+2VOCl2![]() MgCl2+2VOCl,下列说法错误的是
MgCl2+2VOCl,下列说法错误的是
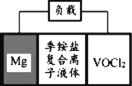
A.采用Mg作电极材料比Li的安全性更高
B.放电时正极反应为VOCl2+e=VOCl+Cl
C.放电过程中Cl穿过复合离子液体向Mg移动
D.为该电池充电时Mg电极应与电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O===O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
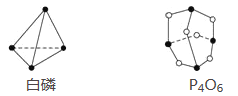
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注。一定温度下,在2L恒容密闭容器中发生反应:2N2O5(g)![]() 4NO2(g)+O2(g) △H>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图。下列说法不正确的是( )
4NO2(g)+O2(g) △H>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图。下列说法不正确的是( )
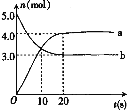
A.0~20s内,平均反应速率v(N2O5)=0.05 mol·L-1·s-1
B.升高温度,可使正逆反应速率均增大
C.达到平衡时,混合气体的压强保持不变
D.10 s时,正、逆反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 L 0.1 mol/L的醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是( )
A. c(CH3COOH)变为原来的1/10
B. c(H+)变为原来的![]()
C. c(CH3COO-)/c(CH3COOH)的比值增大
D. 溶液的导电性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com