
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇?Y2O3?的氧化锆?ZrO2?晶体,在熔融状态下能传导O2?。下列对该燃料电池说法正确的是
A.在熔融电解质中,O2?由负极移向正极
B.电池的总反应是:2C4H10+13O2 ? 8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+4e?+2H2O=4OH?
D.通入丁烷的一极是正极,电极反应为:2C4H10+26e?+13O2?=4CO2+5H2O
科目:高中化学 来源:2017届湖南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
根据下表信息,判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
元素代号 | G | L | M | Q | R | T |
原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
主要化合价 | +1 | +2 | +3 | +6、﹣2 | +5、﹣3 | ﹣2 |
A.单质的还原性:G<L<M B.非金属性:T<Q
C.气态氢化物的稳定性:R>T D.L2+与T2﹣的核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市六校协作体高二上期初考试化学卷(解析版) 题型:选择题
某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+、Al3+ 和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
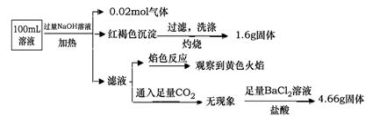
由此可知原溶液中( )
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol·L-1
C.SO42ˉ、NH4+ 、Na+一定存在,CO32ˉ、Al3+一定不存在
D.要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入足量酸性高锰酸钾溶液,若溶液紫红色褪去,则证明原溶液中有Fe2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市六校协作体高二上期初考试化学卷(解析版) 题型:选择题
下列说法不正确的是( )
A.因SiO2不溶于水,故H2SiO3不是SiO2对应的酸或者SiO2不是H2SiO3的酸酐
B.CO2通入水玻璃,可以得到硅酸沉淀
C.SiO2是一种空间立体网状结构的晶体,熔点高,硬度大
D.氢氟酸能够腐蚀玻璃,故不能用玻璃瓶来装氢氟酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上9月月考化学试卷(解析版) 题型:选择题
现有下列两个图像:下列反应中符合两图像的是

A.N2(g)+3H2(g)≒2NH3(g) ΔH<0
B.2SO3(g)≒2SO2(g)+O2(g) ΔH>0
C.4NH3(g)+5O2(g)≒4NO(g)+6H2O(g) ΔH<0
D.H2(g)+CO(g)≒C(s)+H2O(g) ΔH<0
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上9月月考化学试卷(解析版) 题型:选择题
下列事实能用勒夏特列原理解释的是
A.在合成氨的工业生产中,使用较高温度有利于提高产量
B.在合成氨的工业生产中,加压有利于提高氨的产量
C.木炭粉碎后与O2反应,速率更快
D.由H2(g)、I2(g)、HI气体组成的平衡体系加压后颜色变深
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上9月月考化学试卷(解析版) 题型:选择题
一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是 ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量④B物质的量浓度⑤混合气体的摩尔质量
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是 ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量④B物质的量浓度⑤混合气体的摩尔质量
A.①④⑤ B.②③ C.②③④ D.只有④⑤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:选择题
将W1g光亮的铜丝在空气中加热一段时间后,迅速插入下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥,称得其质量为W2 g。实验时由于所插入的物质不同,铜丝的前后质量变化可能不同,下列所插物质与铜丝的质量关系正确的是( )
A.石灰水,W1=W2
B.乙醇溶液,W1=W2
C.NaHSO4,W1<W2
D.CO,W1>W2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:填空题
已知五种短周期元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成四核10电子分子。试回答下列问题:
(1)A、B、C三种离子半径由小到大的顺序是(写离子符号)____________。
(2)C离子的结构示意图是_____________。
(3)用电子式表示A2B的形成过程__________。
(4)写出D元素形成的单质的结构式______________;
(5)写出下列物质的电子式:E2B2__________;D2E4__________;A、B、E形成的化合物__________.
(6)A、B两元素组成的化合物A2B2属于______________(“离子”“共价”)化合物,存在的化学键是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com