
已知某物质的主要成分的化学式为XY2,X原子的结构示意图为,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=________,该物质的化学式为________.
(2)Z、W元素的名称为__________、__________.
(3)下列说法正确的是________.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________.
A.XY2的电子式:X2+[]2-
B.WZ2的结构式:Z===W===Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-===2Y-+Z↓
D.用电子式表示XY2的形成过程为:
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是_____________________________________________________________________.
(1)20 CaCl2 (2)硫 碳 (3)B (4)B、D(5)水分子间存在氢键
解析:根据核外电子的排布规律可知X应是Ca元素,X的阳离子与Y的阴离子的电子层结构相同,所以Y是氯元素。原子的最外层电子数是其电子层数的2倍的,只有C元素和S元素,Z与Y相邻且Z、W能形成一种WZ2型分子,所以Z是S,W是C。
(1)(2)略
(3)CaCl2是离子化合物,只有离子键。CS2是共价化合物,含有极性键,A不正确,B正确。氯但非金属性强于S的,所以氯化氢的稳定性强于硫化氢的,C不正确。钙离子和氯离子具有相同的电子层结构,其微粒半径氯离子的对应钙离子的,D不正确。
(4)CaCl2是离子化合物,只有离子键,电子式为。CS2是直线型结构,B正确。氢硫酸是弱酸,不能改写成离子形成,正确的离子方程式为Cl2+H2S=2H++2Cl-+S↓。钙属于活泼金属,失去电子被氯得到,所以D正确。
(5)由于水中存在氢键,所以其沸点高于硫化氢的。


科目:高中化学 来源: 题型:阅读理解
| 气体 | SO2 | N2 | O2 |
| 物质的量 | 10 | 58 | 6 |
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省抚顺县高级中学高一4月月考化学试卷(带解析) 题型:填空题
已知某物质的主要成分的化学式为XY2,X原子的结构示意图为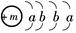 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=________,该物质的化学式为________.
(2)Z、W元素的名称为__________、__________.
(3)下列说法正确的是________.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________.
A.XY2的电子式:X2+[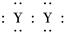 ]2-
]2-
B.WZ2的结构式:Z===W===Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-===2Y-+Z↓
D.用电子式表示XY2的形成过程为: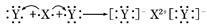
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是_____________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省高一4月月考化学试卷(解析版) 题型:填空题
已知某物质的主要成分的化学式为XY2,X原子的结构示意图为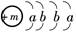 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
(1)m=________,该物质的化学式为________.
(2)Z、W元素的名称为__________、__________.
(3)下列说法正确的是________.
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________.
A.XY2的电子式:X2+[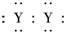 ]2-
]2-
B.WZ2的结构式:Z===W===Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-===2Y-+Z↓
D.用电子式表示XY2的形成过程为: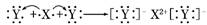
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是_____________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源:09-10年瑞安中学高一提前招阶段性检测化学卷 题型:实验题
已知硫铁矿的主要成分是FeS2(铁元素呈+2价,硫元素呈—1价)。以下是分析硫铁矿中FeS2含量的三种方法,各方法的操作流程图如下:
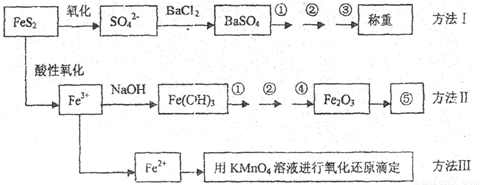
请同答下列问题:
(1)流程图中操作①、②、③分别指的是:①____________、②___________、③________。
操作④、⑤用到的主要仪器是:④_________、⑤__________(每空填1~2个仪器)。
(2)判断溶液中SO42-离子己沉淀完全的方法是______________________________________。
(3)某同学用方法Ⅲ测定试样中Fe元素的含量,需要准确配制KMnO4标准溶液,下列因素导致所配制的溶液浓度偏大的有
A、砝码生锈 B、定容时俯视
C、称量时物质和砝码位置反了(需要游码) D、容量瓶用待装液润
(4)某同学采用方法Ⅱ分析矿石中的Fe含量,发现测定结果总是偏高,则产生误差的可能原因是______________________________________。
(5)称取矿石试样1.60g,按方法Ⅰ分析,称得BaSO4的质量为4.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com