
����Bay�ȹ���ʹ��ʯ�����ѽ�ĸ������������ȡ��������������������ͼ��

(1)�����̵ĵڢ�ӦΪ��CO(g)��H2O(g)H2(g)��CO2(g)���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��________����Ӧ��ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 830 | 1000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | 0.6 |
���ϱ������ƶϣ��˷�Ӧ��________(��������š�)�ȷ�Ӧ��
��830���£�����ʼʱ������ܱ������г���CO��H2O��Ϊ1 mol����ﵽƽ���CO��ת����Ϊ__________��
(2)�����̵ĵ� ��ӦCO(g)��H2O(g)
��ӦCO(g)��H2O(g)  H2(g)��CO2(g)����830�棬���±������ʵ���(��λΪmol)Ͷ����ݷ�Ӧ������������Ӧ�����з�Ӧ��ʼʱ��������Ӧ������е���__________(��ʵ����)��
H2(g)��CO2(g)����830�棬���±������ʵ���(��λΪmol)Ͷ����ݷ�Ӧ������������Ӧ�����з�Ӧ��ʼʱ��������Ӧ������е���__________(��ʵ����)��
| ʵ���� | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
(3)��һ�������ȵĹ̶��ݻ��������У��жϴ����̵ĵڢ�Ӧ�ﵽƽ��ı�־��________(�����)��
����ϵ��ѹǿ���ٷ����仯���ڻ��������ܶȲ���
�ۻ�������ƽ����Է����������䡡�ܸ���ֵ����ʵ���Ũ�Ȳ��ٸı䡡����ϵ���¶Ȳ��ٷ����仯
��v(CO2��)��v(H2O��)
 (4)��ͼ��ʾ�����̵ĵڢ�Ӧ��ʱ��t1�ﵽƽ�⡢��ʱ��t2�ֱ���ı�ij�������������仯�������ͼ��ʱ��t2�����ı��������__________(д������)��
(4)��ͼ��ʾ�����̵ĵڢ�Ӧ��ʱ��t1�ﵽƽ�⡢��ʱ��t2�ֱ���ı�ij�������������仯�������ͼ��ʱ��t2�����ı��������__________(д������)��
������(1)��ƽ�ⳣ�������ֱ��д����Ӧ��ƽ�ⳣ������ʽ���ɱ������ݿ�֪�������¶ȣ�K��С��˵����Ӧ������У�������ӦΪ���ȷ�Ӧ����830��ʱ��K��1���ʿ�����K�����ƽ��ʱC Oת��0.5 mol����CO��ת����Ϊ50%��
Oת��0.5 mol����CO��ת����Ϊ50%��
(2)���������ݴ���K�ı���ʽ��ֻ��B������K<1(830�棬K��1)������ʼʱ��Ӧ������е�ֻ��B�顣
(3)��Ӧ�������������ķ�Ӧ����������̶����ܱ������н��и÷�Ӧ�������Ƿ�ƽ�⣬��������ܶȡ�ƽ����Է���������������ѹǿ�ȶ����䣻�ܢ�˵����ƽ��̬�����֪һ����˵����Ӧ�ﵽƽ�⣻��ϵ���¶Ȳ��ٷ����仯����ӵ�˵������Ӧ���ʵ�Ũ�Ȳ��䡣
(4)��t2ʱCO2��CO��ԭƽ��̬�Ļ����Ϸֱ�Ϊ����ͼ��٣�˵����Ӧ�����ƶ����ʿɲ�ȡ��ʽ�н����¶Ȼ�����ˮ����������������������ȡ�
�𰸣�(1) ���š�50%
���š�50%
(2)B��(3)�ܢݢ�
(4)�����¶Ȼ�����ˮ���������������������


 �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д� �Űٷֿ�ʱ����ϵ�д�
�Űٷֿ�ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴ӦaA(g)��bB(g)  cC(g)��dD(s)����H��Q kJ��mol��1����Ӧ�����У���������������ʱ��C�ڻ�����еĺ������¶�(T)�Ĺ�ϵ��ͼ����ʾ����Ӧ����(v)��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ����ͼ����������˵����ȷ����(����)
cC(g)��dD(s)����H��Q kJ��mol��1����Ӧ�����У���������������ʱ��C�ڻ�����еĺ������¶�(T)�Ĺ�ϵ��ͼ����ʾ����Ӧ����(v)��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ����ͼ����������˵����ȷ����(����)
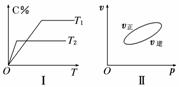
A��T1��T2��Q��0
B������ѹǿ��B��ת���ʼ�С
C������Ӧ�ﵽƽ��ʱ�����������ܶȲ��ٱ仯
D��a��b��c��d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�ϳ���֬�����ֽ�Ϊ��A,1mol A�ܺ�4mol H2�ӳ����ɺ����һ��ı�����C8H16���úϳ���֬Ϊ(����)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
t��ʱ��ijƽ����ϵ�к���X��Y��Z��W�������ʣ����¶��·�����Ӧ��ƽ�ⳣ������ʽΪK�� ���йظ�ƽ����ϵ��˵����ȷ����(����)
���йظ�ƽ����ϵ��˵����ȷ����(����)
A������������ƽ����Է����������ֲ���ʱ����Ӧ��ƽ��
B������ѹǿ�������ʵ�Ũ�Ȳ���
C�������¶ȣ�ƽ�ⳣ��K����
D������X������ƽ��ȿ��������ƶ���Ҳ���������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ȷ�ӦCO(g)��H2O(g)  CO2(g)��H2(g)���¶�t1ʱ�ﵽƽ�⣬c1(CO)��c1(H2O)��1.0 mol/L����ƽ�ⳣ��ΪK1�����߷�Ӧ��ϵ���¶���t2ʱ����Ӧ���ƽ��Ũ�ȷֱ�Ϊc2(CO)��c2(H2O)��ƽ�ⳣ��ΪK2����(����)
CO2(g)��H2(g)���¶�t1ʱ�ﵽƽ�⣬c1(CO)��c1(H2O)��1.0 mol/L����ƽ�ⳣ��ΪK1�����߷�Ӧ��ϵ���¶���t2ʱ����Ӧ���ƽ��Ũ�ȷֱ�Ϊc2(CO)��c2(H2O)��ƽ�ⳣ��ΪK2����(����)
A��K2��K1�ĵ�λ��Ϊmol/L
B��K2��K1
C��c2(CO)��c2(H2O)
D��c1(CO)��c2(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���в���ȷ���ǣ� ( )
A��ά����C���л�ԭ�ԣ�������������������
B��Ϊ��ֹ�±��ȸ�֬ʳƷ�������ʣ����ڰ�װ���з�����������
C����ˮ���������c(H+) = 1��10��13 mol/L����Һ�У�K+��CO32����Cl����NO3�����ܴ�������
D��ʹʯ�������Һ�У� Na+��I����Cl����NO3�����ܴ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Դ���������Ϊ��Լ������ᾭ�÷�չ��ƿ����Խ��Խ��Ĺ��ҿ�ʼʵ�С�����ƻ���������̫������Դ��Ѱ�÷�չ���¶�����
��1��̫������ˮ���г�ʹ��һ�����������Ͻ������Ϊ���ռ���̫��������Ϳ�㣬д����̬��ԭ�ӵ���Χ�����Ų�ʽ__________����λ�����ڱ�____________����
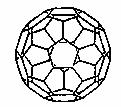
��2�� ����ϩ���������ھ������õĹ�����ܣ���̫���ܵ�ص�Ӧ���Ͼ��зdz�������ǰ;������ϩ��C60���Ľṹ����ͼ��������̼ԭ�ӹ�����ӻ�����Ϊ________��1 mol C60�����ЦҼ�����ĿΪ____________����
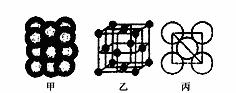
��3��Cu���ʾ�����ԭ�ӵĶѻ���ʽ����ͼ����ʾ���侧����������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ����ͼ����ʾ��������Cuԭ�ӵ���λ��Ϊ____________��һ��������Cuԭ�ӵ���ĿΪ________��
��4��Fe��CO��5�����³�Һ̬���۵�Ϊ��20��5 �棬�е�Ϊ103 �棬�����ڷǼ����ܼ����ݴ˿��ж�Fe��CO��5��������________��������ͣ���Fe��CO��5���������壮��λ���ֱ���________��________��
��5������˵����ȷ����________��
A����һ�����ܴ�С��S��P��Si
B���縺��˳��C��N��O��F
C����Ϊ������CaO��KCl�ߣ�����KCl��CaO�۵��
D��SO2��CO2�Ļ�ѧ�������ƣ����ӽṹҲ����ֱ���ͣ���ͬ������SO2���ܽ�ȸ���
E�����Ӿ����У����ۼ�����Խ�÷��Ӿ�����ۣ��е�Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪H��H������Ϊ436 kJ/mol��H��N������Ϊ391 kJ/mol�����ݻ�ѧ����ʽ��
N2(g)��3H2(g)===2NH3(g)����H����92 kJ/mol����N��N�ļ����� (�� ��)
A��431 kJ/mol B��946 kJ/mol
C��649 kJ/mol D��869 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и������ӣ�һ������ָ�������д����������
A�����д���I�����ӵ���Һ�У�
Cl����Fe3����Al3����Cu2��
B��ʹ���ȱ�����Һ�У�
Fe3����Na����SO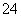 ��NO
��NO
C����ˮ�������c(H��)��10��12 mol��L��1����Һ�У�
Na����Ba2����AlO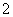 ��HCO
��HCO
D������Al�ܷų�����H2����Һ�У�
NH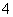 ��K����SO
��K����SO ��Cl��
��Cl��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com