
| ��� | ���������� | ���� |
| A | ��0.1mol?L-1��ˮϡ�ͳ�0.01mol?L-1�����pH��11.1���10.6 | ϡ�ͺ�NH3?H2O�ĵ���̶ȼ��� |
| B | ��ij��ɫ��Һ�еμ�ϡ���������μ��Ȼ�����Һ��������ɫ���� | ����Һ��һ������SO42- |
| C | ��ij����ͨ��Ʒ����Һ��Ʒ����Һ��ɫ | ������һ����SO2 |
| D | ��ZnS�����ϵμ�����ͭ��Һ��������Ϊ��ɫ | ͬ���£�KsP��ZnS����KsP��CuS�� |
| A��A | B��B | C��C | D��D |


 ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Ӱ뾶��r��E����r��B����r��C�� |
| B���۵㣺CE��DE4 |
| C��C��B�γɵ����ֻ������л�ѧ�����Ͳ�ͬ |
| D��A��D��E������������Ӧˮ�������������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
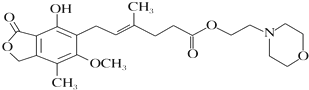
| A��ù������������ˮ |
| B��ù����������Ũ��ˮ����ȡ����Ӧ |
| C��1molù���������뺬4mol NaOH��ˮ��Һ��ȫ��Ӧ |
| D��ù�������ȿ��Դ����⣬�ֿ���ʹ����KMnO4��Һ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��MnO2��Ũ���ᷴӦ��Cl2��MnO2+4HCl
| ||||
| B��Na2S2O3��Һ�м���ϡ���2S2O32-+4H+�TSO42-+3S��+2H2O | ||||
| C��˫��ˮ�м���ϡ�����KI��Һ��H2O2+2H++2I-�TI2+2H2O | ||||
| D����������������ϡ���3Fe2++4H++NO3-�T3Fe3++NO��+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
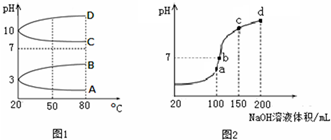
 ��ͼ��һˮ��Һ��pH��0��14�ķ�Χ�ڣ�H2CO3��HCO3-��CO32-���ֳɷ�ƽ��ʱ����ɷ���������������ȷ���ǣ�������
��ͼ��һˮ��Һ��pH��0��14�ķ�Χ�ڣ�H2CO3��HCO3-��CO32-���ֳɷ�ƽ��ʱ����ɷ���������������ȷ���ǣ�������| A����ͼ��1.0mol/L̼������Һ�ζ�1.0mol/L HCl��Һ�ĵζ����� |
| B����pHΪ6.37��10.25ʱ����Һ��c��H2CO3��=c��HCO3-��=c��CO32-�� |
| C������ѪҺ��pHԼΪ7.4����CO2��ѪҺ�ж���HCO3-����ʽ���� |
| D������CO2��NaOH��Ӧ��ȡNa2CO3����Һ��pH���������12���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaHCO3��Һ������Fe2��SO4��3��Һ��Ӧ��Fe3++3HCO3-�TFe��OH��3��+3CO2�� |
| B������NaOH��Һ��NH4HS��Һ��Ӧ��OH-+NH4+�TNH3?H2O |
| C����Br2ˮ�м���������Na2SO3��Һ��Br2+SO32-+H2O�TSO42-+2H++2Br- |
| D�����Ȼ�����Һ��ͨ�������Ķ�����̼��Ca2++CO2+H2O�TCaCO3��+2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ش��� | X | Y | Z | W |
| ԭ�Ӱ뾶/nm | 0.186 | 0.089 | 0.074 | 0.099 |
| ��Ҫ���ϼ� | +1 | +2 | -2 | +7��-1 |
| A��X��YԪ�صĽ����ԣ�X��Y |
| B��X��Z�γɵĻ�������һ���������ۼ� |
| C��W������������ˮ������һ��ǿ�� |
| D�����Ӱ뾶��X+��Z2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com