
| A��0.1 mol��L��1 Na2CO3��Һ��c(Na+)=2c(HCO3��)+2c(CO32��)+2c(H2CO3) |
| B��0.1 mol��L��1 NH4Cl��Һ��c(NH4+)=c(Cl��) |
| C�����������Һ�м����������ᣬ�õ������Ի����Һ��c(Na+) > c(CH3COO��) > c(H+) > c(OH��) |
| D�������£���pH=2�������pH=12�İ�ˮ�������Ϻ�c(NH4+) > c(Cl��) > c(OH��) > c(H+) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH=4�Ĵ����У�c(H+)=4.0mol?L��1 |
| B������С�մ���Һ�У�c(Na+)= c(HCO3��) |
| C������ʳ��ˮ�У�c(Na+)+ c(H+)= c(Cl��)+c(OH��) |
| D��pH=12�Ĵ�����Һ�У�c(OH��)=1.0��10��2mol?L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
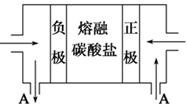
| ���� | CH3COONa | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 11.6 | 10.3 | 11.1 |
| ���� | Fe2�� | Cu2�� | Mg2�� |
| pH | 7.6 | 5.2 | 10.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Һ�е������ӵ���Ŀ���� |
B����Һ��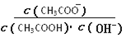 ���� ���� |
| C������ĵ���̶�����c(H��)������ |
| D���ټ���10 mL pH��11��NaOH��Һ�����ҺpH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1mol/LCH3COONa��0.1mol/LHCl��Һ�������ϣ�c(Na��)��c(Cl��)��cCH3COO��)��c(OH��) |
| B��0.1mol/LNH4Cl��0.1mol/L��ˮ�������ϣ�pH��7����c(NH3��H2O)��c(NH4��)��c(Cl��)��c(OH��) |
C��0.1mol/LNa2CO3��0.1mol/L NaHCO3��Һ�������ϣ� c(Na��)��c(CO32��)��c(HCO3��)��c(H2CO3) c(Na��)��c(CO32��)��c(HCO3��)��c(H2CO3) |
| D��0.1mol/LNa2C2O4��0.1mol/LHCl��Һ�������ϣ�H2C2O4Ϊ��Ԫ���ᣩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��b��c������Һ�ĵ���������ͬ |
B��c����Һ�� |
| C��a��b��c������Һ��ˮ�ĵ���̶�a>c>b |
D������ͬŨ�ȵ�����ֱ���������b��c����Һ��Ӧ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����A�ܼ��У������Դ����ң���B���ܼ��У������Կ���С���� |
| B���Ƚ�HCl��H2SO4��HClO4��HNO3���Ե�ǿ������ˮ�϶������ԣ��ñ�������ܿ��� |
| C��HNO3��HClO4�����ᣬ��H2SO4�п����Ǽ� |
| D���Ƚ�HCN��HAc���Ե�ǿ������ˮ�϶����ԣ���Һ���϶�Ҳ���� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com