
| A.CO2不能与CaCl2溶液反应,则SO2也不能与CaCl2溶液反应 |
| B.金属钠着火不能用CO2扑灭,则金属钾着火也不能用CO2扑灭 |
| C.乙烯能使酸性KMnO4溶液褪色,则丙烯也能使酸性KMnO4溶液褪色 |
| D.Al(OH)3能与NaOH溶液反应,则Al(OH)3也能与氨水反应 |
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源:不详 题型:实验题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
| 分装时期 | |
| 分装企业 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带有两个单位的负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子具有相同的电子层结构,且核电荷数与B相差 3 3 |
| D | 与C同周期,且最外层电子是C的3倍 |
| E | 与D同周期,原子半径在该周期中最小 |
 )写出电解CE溶液的化学方程式:
)写出电解CE溶液的化学方程式: 本题共7分)
本题共7分)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
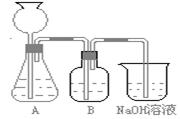
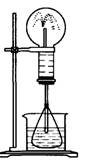
 (5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
(5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。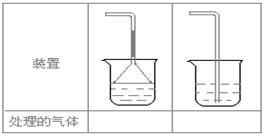
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
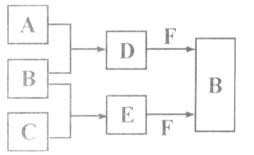
 。Z和酸性碘
。Z和酸性碘 化钾溶液反应生成B和碘单质,反应的离子方程式是 。
化钾溶液反应生成B和碘单质,反应的离子方程式是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
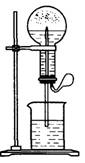
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将SO2通入BaC12溶液中 | B.将C12通入AgNO3溶液中 |
| C.将NH3通入AgNO3溶液中 | D.将NO2通入Ca(OH)2溶液中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在水电离出的c(H+)与c(OH-)乘积为10-28的溶液中能大量共存是:K+、Na+、HCO-3、Ca2+ |
| B.乙烯和环丙烷(C3H6)组成的28g混合气体中含有4×6.02×1023 个氢原子 |
| C.将铂丝用盐酸洗净后,在酒精灯的外焰上灼烧至没颜色,蘸取碳酸钾固体,再在酒精灯外焰灼烧,进行钾的焰色反应 |
| D.0.1mol·L-1CH3COOH溶液中,加水冲稀,电离平衡向电离方向移动,电离平衡常数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com