
X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大。其相关信息如下表所示:
|
X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
|
Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
|
Z元素的族序数是其周期数的三倍 |
|
W原子的第一至第六电离能分别为:I1=578KJ·mol-1 I2=1817KJ·mol-1 I3=2745KJ·mol-1 I4=11575KJ·mol-1 I5=14830KJ·mol-1 I6=18376KJ·mol-1 |
|
Q为前四周期中电负性最小的元素 |
|
元素R位于周期表的第10列 |
回答下列问题:
(1)Y元素的基态原子中未成对电子数为______;X、Y、Z三种元素原子的第一电离能由小到大的顺序为____________(用元素符号表示)。
(2)W的氯化物的熔点比Q的氯化物的熔点__________(填“高”或“低”),理由是__________________________________________________。
(3)光谱证实元素W的单质与强碱性溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在(填字母)_____________。
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
(4)含有X、R和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为 ;晶体中每个镁原子周围距离最近的R原子有 个。

(1)3(2分) C O N(2分)
(2)低 (2分) W的氯化物为分子晶体,Q的氯化物为离子晶体(3分)
(3)ac (2分) (4)MgNi3C (2分) 12(2分)
【解析】
试题分析:X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同,说明是1s22s22p2,就是C,Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应,是N,Z元素的族序数是其周期数的三倍,是O,根据W的电离能第一、二、三数据小确定是Al,Q为前四周期中电负性最小的元素K,元素R位于周期表的第10列,第四周期,是Ni。(1)N1s22s22p3,未成对电子数为3,(4)根据分摊原则,可以确定分子式MgNi3C
考点:考查元素周期表、物质结构、化学键


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
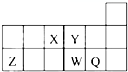 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )| A、元素Y最高正化合价与最低负化合价的绝对值之和的数值等于8 | B、原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q) | C、离子Y2-和Z3+半径的大小顺序为:r(Y2-)>r(Z3+) | D、元素W的最高价氧化物对应的水化物的酸性比Q的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com