
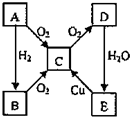
 A、B、C、D、E各物质的转化关系如图所示.
A、B、C、D、E各物质的转化关系如图所示. CaCl2+2NH3↑+2H2O,氨气是碱性气体,不能与浓硫酸做干燥剂,
CaCl2+2NH3↑+2H2O,氨气是碱性气体,不能与浓硫酸做干燥剂, CaCl2+2NH3↑+2H2O;不能;
CaCl2+2NH3↑+2H2O;不能; 2SO3,故答案为:2SO2+O2
2SO3,故答案为:2SO2+O2 2SO3;
2SO3; CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4 (浓)
CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4 (浓) CO2↑+2SO2↑+2H2O.
CO2↑+2SO2↑+2H2O.

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
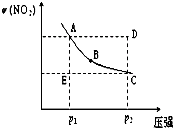 (2009?汕头二模)对于反应N2O4(g)
(2009?汕头二模)对于反应N2O4(g)  2NO2(g)在温度一定时,平衡体系中NO2的体积分数ψ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是( )
2NO2(g)在温度一定时,平衡体系中NO2的体积分数ψ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
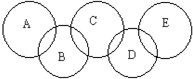 如图,A、B、C、D、E各代表碳、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质.一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:
如图,A、B、C、D、E各代表碳、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质.一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)该反应的正反应方向是一个
(1)该反应的正反应方向是一个查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | |
| A | ↓ | - | ↓ | - | |
| B | ↓ | ↓ | - | ||
| C | - | ↓ | ↑ | - | |
| D | ↓ | ↓ | ↑ | ↓ | |
| E | - | - | - | ↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com