
【题目】下列关于原子结构的表述中,正确的是( )
A.L能层含轨道数共有8个
B.在基态K原子中,核外电子占据最高能级符合为N
C.电子云轮廓图半径随能层序数增加而增大
D.根据洪特规则每个轨道最多容纳2个自旋状态相反的电子
科目:高中化学 来源: 题型:
【题目】下列有关组成生物体细胞的化学元素的叙述,错误的是
A. 构成细胞的最基本元素是碳
B. H7N9病毒和桃树共有的元素是C、H、0、N、P等
C. 生物体内含有的元素都是生物体所必需的
D. Cu、Mn、Mo、B都是组成生物体的微量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知-C6H5 代表苯基,下列卤代烃在 KOH 醇溶液中加热能发生消去反应的有( )种
① C6H5Br ②CH3Cl ③(CH3)3CCH2Cl ④C6H5CH2Br ⑤ CHCl2-CHBr2 ⑥(CH3)3CCl
A.1B.2C.3D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯净物X、Y、Z转化关系如图所示,下列判断正确的是( )

A. X可能是金属铜 B. Y不可能是氢气
C. Z可能是氯化钠 D. Z可能是三氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NH3、CO、Na、Na2O2、Fe、NO、NO2、F2、SO2、SOCl2等中学化学教材中出现过的物质,根据它们的组成及性质进行如下分类:

请回答下列问题:
(1)图中所示的分类方法叫________。
(2)淡黄色固体最终位于________组,它的电子式为____________。
(3)C组有一种气体常用作工业上冶炼铁的还原剂,写出高温下它还原Fe2O3的化学方程式:________________。
(4)Ⅱ组某种物质能与水发生氧化还原反应,该反应中被氧化与被还原的元素的质量比为________。
(5)B组中有一种物质在高温下能与水蒸气反应,若该反应过程中有8×6.02×1023个电子转移,则有________g该物质参与反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室安卡因(G)是一种抗心律失常药物,可由下列路线合成:
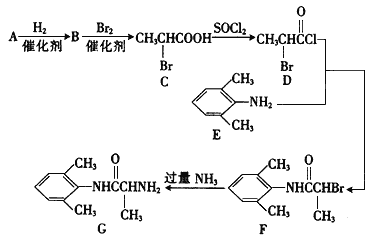
I.(1)己知A是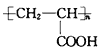 的单体,则A中所含官能团的名称是____________。
的单体,则A中所含官能团的名称是____________。
(2)写出B的结构简式并用系统命名法给C命名: B:_____________, C的名称:____________。
(3)L是E的同分异构体,L分子中含有苯环,且苯环上一氯代物只有两种,则L所有可能的结构简式有![]() 、__________________。
、__________________。
(4)F →G的反应类型是_______________。
(5)下列关于室安卡因(G)的说法正确的是____________。
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d.属于氨基酸
(6)写出C与足量NaOH醇溶液共热时反应的化学方程式:______________。
II. H是C的同系物,其核磁共振氢谱有两个峰。按如下路线,由H可合成高聚物V:
![]()
(7)H的结构简式为_________________;N→Q的反应类型为________________。
(8)写出Q→V的反应方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对Na、Mg、Al的有关性质的叙述正确的是:
A. 碱性:NaOH< Mg(OH)2< Al(OH)3 B. 第一电离能:Na< Mg <Al
C. 电负性:Na> Mg >Al D. 还原性:Na> Mg >Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为几种晶体或晶胞的示意图:
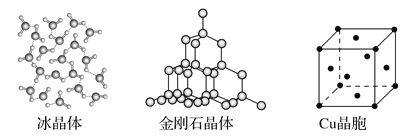
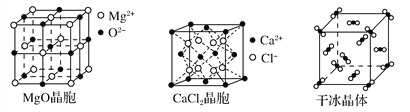
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为________________________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能______(填“大于”或“小于”)MgO晶体,原因是________________________________________________。
(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com