
氢化铝钠(NaAlH4)是最冇研究应用前景的络合金属氢化物,氢化铝钠储放氢时发生反应:3NaAlH4 Na3AlH6+2Al+3H2↑。下列说法正确的是
Na3AlH6+2Al+3H2↑。下列说法正确的是
| A.NaAlH4中氢元素为+1价 |
| B.每生成11. 2 L(标准状况下)H2,转移2NA个电子 |
| C.在反应中有50%的氢被氧化 |
| D.反应中氧化产物与还原产物的物质的量之比为1: 1 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
下列关于置换反应:X+Y=W+Z(反应条件已经略去)的叙述正确的是( )
| A.若X是金属单质,则W和Z中一定有一种物质是金属单质 |
| B.若X是非金属单质,则W和Z中一定有一种物质是非金属单质 |
| C.若X是含有金属元素的化合物,则W和Z中一定有一种是含有金属元素的化合物 |
| D.若X是不含有金属元素的化合物,则W和Z中一定有一种物质是非金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将0.195g锌粉加入到20mL 0.100 mol?L—1MO2+溶液中,恰好完全反应,则还原产物可能是
| A.M | B.M2+ | C.M3+ | D.MO2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于阴影部分的是( )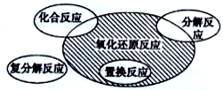
| A.Cl2+2KBr=Br2+2KCl |
B.2NaHCO3  Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
H2O2是在医疗、化工方面应用广泛的化学试剂。
(1)Na2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,则应选择的过氧化物是________;
(2)实验室可用H2O2与次氯酸钠反应制氧气,其中还原剂是__________,写出该反应的化学方程式 ,生成0.5mol氧气,转移电子_______mol;
(3)用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:
H2O2 + KMnO4 + H2SO4 → MnSO4 + K2SO4 + O2↑ + H2O ,若滴定中消耗0.50mol/L的高锰酸钾溶液40.00ml,则此双氧水溶液中溶质的质量为____________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
置换反应的通式可以表示为:
单质(1)+化合物(1)= 单质(2)+化合物(2)
请联系所学过的单质 (如H2、C、Si、Cl2、Br2、I2、Na、Mg、Al、Cu、Fe等)的性质,写出满足以下条件的化学方程式(各写一个)。
(1)单质(1)和单质(2)都是金属: ;
(2)单质(1)是金属,而单质(2)是非金属: ;
(3)单质(1)是非金属,而单质(2)是金属: ;
(4)单质(1)和单质(2)都是非金属: 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。则下列说法错误的是
| A.反应过程中,被氧化与被还原的元素的物质的量之比为1:2 |
| B.NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C.若反应中转移的电子数目为6.02×1023,则可生成22.4L NO气体(标准状况) |
| D.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4==2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3==2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中均为硫元素被氧化 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
| C.氧化性:MnO2>SO42->IO3->I2 |
| D.反应①、②中生成等量的I2时转移电子数比为1∶5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有Fe2+、NO-3、Fe3+、NH+4、H+和H2O六种微粒,分别属于同一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
| A.氧化剂与还原剂的物质的量之比为8:1 |
| B.还原产物为NH+4 |
| C.若有l mol NO-3参加还原反应,则转移8mol e- |
| D.若把该反应设计为原电池,则负极反应为Fe2+—e-=Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com