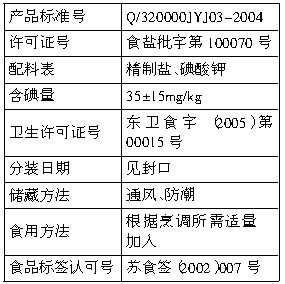
下表是江苏省某县超市出售的“淮牌”加碘精制盐的有关说明。
Ⅱ.下面是某网站上刊出的有关碘及其化合物的有关信息。
自然界中碘主要以碘化物和碘酸盐的形式存在。碘在海水中的含量甚微,但海洋中某些生物如海带、海藻等具有选择性吸收和聚集碘的能力,因而干海藻是碘的一个重要来源。目前世界上碘主要来自于智利硝石,其中含碘0.02%~1%,智利硝石中碘主要以碘酸钠(NaIO
3)的形式存在。通常情况下碘是一种紫黑色固体,易升华,只能少量溶于水得棕黄色的碘水溶液,但易溶于苯、四氯化碳等有机溶剂,紫色的碘蒸气有刺激性气味,能强烈刺激眼、耳、鼻、气管等黏膜,吸入较多的碘蒸气会发生中毒,甚至造成死亡。碘遇淀粉(面粉的主要成分)会出现明显的蓝色。碘离子(I-)具有明显的还原性,而高价态的碘则具有较强的氧化性:
①2NaI+3H
2SO
4+MnO
2=2NaHSO
4+MnSO
4+2H
2O+I
2②2NaIO
3+5NaHSO
3=2Na
2SO
4+3NaHSO
4+H
2O+I
2反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应。
根据以上信息,回答下列问题:
(1)写出有关反应的离子方程式(已知:NaHSO
3=Na++ HSO
3-):反应①:__________;反应②:________;I
2在反应①中是______________(填“氧化”或“还原”,下同)产物,在反应②中是__________________产物。
(2)请你设计实验探究上述“淮牌”精制盐中是否真的含有碘元素。
实验名称:探究“淮牌”精制盐中是否含有碘元素。
实验目的:1.认识碘酸钾中的碘元素转变成碘单质的化学反应;
2._________________________。
实验原理:____________________(提示:结合题中信息和实验目的进行分析)。
实验用品:____________________(提示:实验用品通常包括仪器和药品,根据你设计的实验填写)。
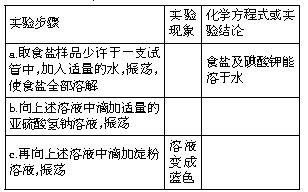
实验步骤:(用准确、简洁的语言填写下表)






 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案