
| A. | 都是共价化合物 | B. | 都是离子化合物 | C. | 互为同分异构体 | D. | 互为同系物 |
分析 A.氰酸铵(NH4OCN)属于离子化合物;
B.尿素[CO(NH2)2]属于共价化合物;
C.分子式相同结构不同的化合物属于同分异构体;
D.结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物.
解答 解:A.氰酸铵(NH4OCN)属于铵盐,是离子化合物,故A错误;
B.尿素[CO(NH2)2]中只含共价键,属于共价化合物,故B错误;
C.氰酸铵(NH4OCN)与尿素[CO(NH2)2]的分子式相同但结构不同,所以属于同分异构体,故C正确;
D.氰酸铵(NH4OCN)与尿素[CO(NH2)2]的分子式相同,分子组成不相差CH2原子团,不是同系物,故D错误;
故选C.
点评 本题考查基本概念,明确这几个概念的含义是解本题关键,注意同系物、同分异构体的区别,难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:解答题
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:Na>Mg | B. | 热稳定性:HF>HCl | ||
| C. | 酸性:H2SO3>H2CO3 | D. | 氧化性:O2>S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 氧化铜和氧化亚铜都是黑色固体 | |
| C. | 铝在高温下能还原锰、铁、铬等金属氧化物得到金属 | |
| D. | 因为镁和铝在空气中都能形成氧化膜,所以镁铝都不能溶于浓盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
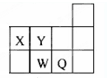
| A. | 元素X与元素Y可形成多种化合物 | |
| B. | 原子半径的大小顺序为:X>Y>W>Q | |
| C. | 还原性:W2-<Q- | |
| D. | 元素W的最高价氧化物对应水化物的酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
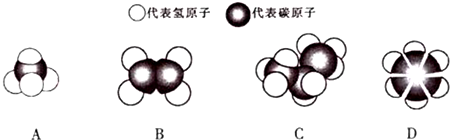
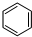 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$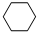 .
. .
.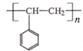 路线流程图(无机试剂任选).合成路线流程图示例如下:
路线流程图(无机试剂任选).合成路线流程图示例如下: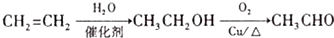
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
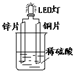
| A. | 锌片换成铁片,电路中的电流方向不变 | |
| B. | 铜电极的电极反应式为Cu2++2e-=Cu | |
| C. | 将硫酸换成柠檬汁,导线中仍有电子流动 | |
| D. | 装置中存在“化学能→电能→光能”的转换 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
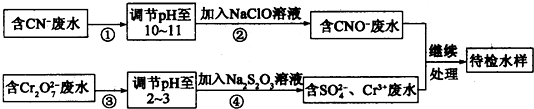
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com