
【题目】一定条件下,NO跟NH3可以发生反应生成N2和H2O,6NO+4NH3=5N2+6H2O,现有NO和NH3的混合物1mol,充分反应后所得产物中,若经还原得到的N2比经氧化得到的N2多1.4g。
(1)在方程式中标出电子转移的方向和数目。6NO+4NH3=5N2+6H2O;
(2)若以上反应进行完全,试计算原反应混合物中NO与NH3的物质的量的比为 。
【答案】(1)
(2)(6分)3:7;4:1
【解析】
试题分析:(1)NO跟NH3可以发生反应生成N2和H2O ,根据电子守恒、原子守恒,可得反应的化学方程式:6NO+4NH3=5N2+6H2O。在该反应中,N元素的化合价由反应前NO中的+2价变为反应后N2中的0价,化合价降低2,获得2个电子,N元素的化合价由反应前NH3中的-3价变为反应后N2中的0价,化合价升高3,失去3个电子,根据化合价升降总数相等,等于元素化合价升降总数,可知NO的系数是3,NH3的系数是2,反应产生的N2的系数是5/2,H2O的系数是3,然后都扩大2倍,变为整数系数,可得该反应的电子转移表示式: ;
;
(2)在反应方程式为6NO+4NH3=5N2+6H2O,该反应中氧化产物和还原产物都是氮气,根据方程式可知:若有6molNO发生反应,会消耗4molNH3,产生5molN2,还原产物比氧化产物多1mol,现在还原产物比氧化产物多1.4g,则还原产物比氧化产物多1.4g÷28g/mol=0.05mol,反应的NO的物质的量是0.3mol,反应的氨气的物质的量是0.2mol。由于二者的物质的量的和是1mol,所以过量的气体的物质的量是1mol-0.2mol-0.3mol=0.5mol。假设NO完全反应,则NO的物质的量=(0.05mol÷1)×6=0.3mol,氨气的物质的量是n(NH3)=1mol-0.3mol=0.7mol;假设氨气完全反应,则NH3的物质的量是0.2mol,则NO的物质的量=1mol-(0.05mol÷1)×4=0.8mol,所以原反应混合物中NO与NH3的物质的量可能0.3molNO和0.7molNH3或0.2molNH3和0.8molNO,因此原反应混合物中NO与NH3的物质的量的比为3:7或4:1。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】生活中的问题常涉及化学知识,下列过程不涉及化学变化的是( )
A. 用食醋除去暖瓶内的水垢
B. 用四氯化碳擦去圆珠笔油渍
C. 用糯米饭、酒曲等自制甜酒酿
D. 用纯碱清除炊具上残留的油污
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像能表示相关反应中生成物物质的量的变化的是(横、纵坐标单位:mol) ( )。
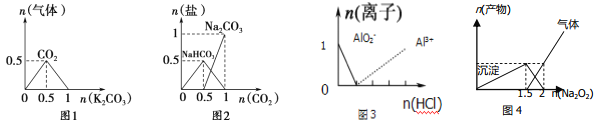
A.图1:n(HCl)=l mol,K2CO3加入到HCl溶液中,在敝口容器中生成的气体
B.图2:n(NaOH)=1mol,CO2通入到NaOH溶液中反应生成的盐
C.图3:n(NaAlO2)=1 mol,HCl加入到NaAlO2溶液中离子的存在情况
D.图4:n(AlCl3)=1 mol,Na2O2加入AlCl3溶液反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl- 六种粒子。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是
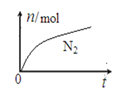
A. 该反应的还原剂是Cl-
B. 消耗1 mol还原剂,转移6 mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已严重已严重危害人类的生活。下列对应关系正确的是
选项 | 环境问题 | 造成环境问题的主要物质 |
A | 酸雨 | O3 |
B | 温室效应 | CO2 |
C | 南极臭氧层空洞 | SO3 |
D | 光化学烟雾 | N2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
(1)有下列十种物质:
A.空气
B.O2
C.NaHSO4
D.氨水
E.CuSO4
F.NaOH
G.CO2
H.Fe2O3
I.金刚石
J.H2SO4
其中属于非电解质的有 ;属于盐的有 。(填字母)
(2)有下列六个反应:
A.Cl2+H2O=HCl+HClO
B.Zn+H2SO4=ZnSO4+H2↑
C.2Cu2O+Cu2S![]() 6Cu+SO2↑
6Cu+SO2↑
D.Cl2+2KI=2KCl+I2
E.H2+Cl2===2HCl
F.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
其中既属于分解反应又属于氧化还原反应的是 (填字母)。
(3)K2FeO4是一种重要的净水剂,可用下列方法制得:
2Fe(OH)3+3Cl2+10KOH![]() 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O
在该反应中,还原剂是 (填化学式),当反应中有1mol K2FeO4生成时,转移电子的数目为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com