
用浓H2SO4在加热条件下跟草酸晶体作用,可制取CO,其反应为:
H2C2O4·2H2O CO↑+CO2↑+3H2O
CO↑+CO2↑+3H2O
再利用制得的干燥CO还原Fe2O3粉末制取还原铁粉,并验证CO被Fe2O3氧化后的产物是CO2,请利用图中的装置和药品设计一个实验完成上述实验任务.
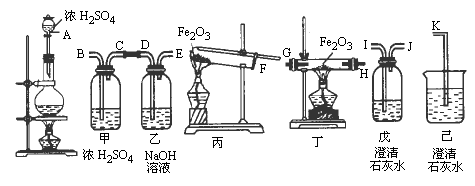
请回答下列问题:
(1)从图中选用必要的装置,完成上述实验.所选仪器的连接顺序是(用各接口的代码字母填写)________接________、________接________、________接________、________接________.
(2)实验中两次用到浓H2SO4,在这两处浓H2SO4的作用(按发生反应的先后)分别是________和________.从气体发生装置中产生的气体跟Fe2O3反应前应经过装置________和________,其作用分别是________和________.
(3)从盛Fe2O3的装置中排出的气体须经过装置________,其目的是________,实验后的尾气须经过________处理,这样处理的理由是________.
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014届黑龙江省高一上学期期末考试化学试卷 题型:实验题
(12分)某化学兴趣小组为了探究锌与浓硫酸反应生成气体的成分做了如下实验:
将50g锌粉与50mL浓H2SO4在加热条件下充分反应,锌粉有剩余,收集到一定体积的气体,将该气体体积折算成标准状况为11.2L。
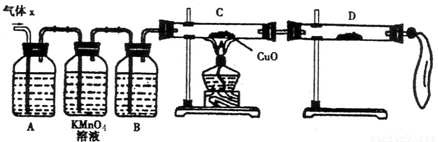
(1) 化学兴趣小组所制得的气体X中混有的主要杂质气体可能是
(填分子式)。产生这种结果的主要原因是(用离子方程式表示) 。
(2)实验验证:为了检验主要杂质气体的成分,化学兴趣小组的同学设计了如下实验,对气体X取样进行探究。
①A中加入的试剂可能是 ,作用是 。
B中加入的试剂可能是 。
②证实气体X中混有杂质气体,D中应选择的试剂是 ,同时应观察到C中的实验现象是 。
(3)理论分析:
①该小组有同学提出只需要再测出一个数据,便能准确的确定该气体的组成,你认为他可以是测下列 。
A、反应后剩余锌的质量为17.5g
B、收集到气体的质量为25.8g
C、浓硫酸的物质的量浓度为18.0mol/L
②根据你在①中所选数据,通过计算确定气体X中各成分物质的量分别为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com