
 写出下列反应的热化学方程式
写出下列反应的热化学方程式分析 (1)根据N2(g)与H2(g)反应生成1mol NH3(g),放出46.1KJ热量,则1molN2(g)与3molH2(g)反应生成2mol NH3(g),放出46.1×2KJ热量,据此书写;
(2)根据0.5mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出445kJ的热量,则1mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出890kJ的热量,据此书写;
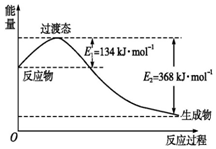
(3)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(4)已知:①CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,
根据盖斯定律,②-①可得.
解答 解:(1)因为N2(g)与H2(g)反应生成1mol NH3(g),放出46.1KJ热量,则1molN2(g)与3molH2(g)反应生成2mol NH3(g),放出46.1×2KJ热量,所以反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ•mol-1;故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ•mol-1;
(2)因为0.5mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出445kJ的热量,则1mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出890kJ的热量,所以反应的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△=-890kJ•mol-1;故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△=-890kJ•mol-1;
(3)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量为:368-134=234kJ,
反应热化学方程式为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1 .
故答案为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1 ;
(4)已知:①CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,
根据盖斯定律,②-①可得:CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol-1 ,
故答案为:CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol-1 .
点评 本题考查了热化学方程式的书写,题目难度中等,注意掌握盖斯定律的应用和热化学方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的消耗速率与B的生成速率相等 | |
| B. | 单位时间内消耗3a mol C,同时生成a mol A | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体的密度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸溶液与氢氧化钡溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| B. | 硫酸与氢氧化镁溶液:H++OH-═H2O | |
| C. | 碳酸钙与稀硝酸:CO32-+2H+═CO2↑+H2O | |
| D. | 铁与稀硫酸反应:Fe+2H+═Fe2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2晶体中共含有4NA个离子 | |
| B. | 0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 | |
| C. | 常温常压下16gO2和O3混合气体含有NA个氧原子 | |
| D. | 1mol/LNa2CO3溶液中含有NA个CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com