
【题目】下列说法不正确的是( )
A.MCl2在水溶液中的电离方程式为:MCl2 = M2+ + 2Cl-,则M(OH)2可能是弱电解质
B.足量的锌分别与等体积的盐酸(pH = 1)和醋酸(0.1molL-1)反应,在相同条件下产生的氢气体积相同
C.NaHSO3溶液显酸性的原因是HSO3-的电离强于水解
D.pH相同的氨水和氢氧化钠加水稀释相同倍数后,![]()
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图,在光照条件下,将盛有CH4和Cl2的量筒倒扣于盛有饱和食盐水的水槽中进行实验,对实验现象及产物分析中错误的是__________。

A.混合气体的颜色变浅,量筒中液面上升
B.量筒内壁上出现的油状液滴,应是三氯甲烷、四氯甲烷的混合物
C.水槽中有白色固体物质析出
D.甲烷与氯气反应后的产物只有CCl4
Ⅱ.根据烯烃的性质回答下列问题。
(1)一瓶无色气体,可能含有CH4和CH2=CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?___________。
②上述实验可能涉及的反应类型有_____。
(2)含有 的化合物与CH2=CH2一样,在一定条件下可聚合成高分子化合物。
的化合物与CH2=CH2一样,在一定条件下可聚合成高分子化合物。
①广泛用作农用薄膜的聚氯乙烯塑料,是由 聚合而成的,其化学方程式是___________________。
聚合而成的,其化学方程式是___________________。
②电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯( ),它是由________(写结构简式)聚合而成的。
),它是由________(写结构简式)聚合而成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组利用文献资料设计方案对氯及其化合物进行探究。
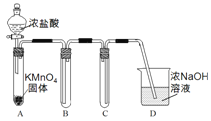
Ⅰ.用高锰酸钾和浓盐酸反应制取氯气
(1)该小组利用右图装置及试剂制备并收集适量Cl2,装置B、C的作用分别是___________、_______________。
(2)制得的氯气中加入适量水,得到饱和氯水,饱和氯水中含氯元素的微粒有____________(写出全部微粒)。
(3)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一。在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强。
①滤液漂白性增强的原因是________________(用化学平衡移动原理解释)。
②饱和氯水与石灰石反应生成HC1O的方程式是___________________。
Ⅱ. ClO3—、Cl—和H+反应的探究
(4)KClO3、KCl与硫酸可以反应。该小组设计了系列实验研究反应条件对反应的影响,实验记录如下(实验在室温下进行):
烧杯编号 | 1 | 2 | 3 | 4 |
氯酸钾饱和溶液 | 1mL | 1mL | 1mL | 1mL |
氯化钾固体 | 1g | 1g | 1g | 1g |
水 | 8mL | 6mL | 3mL | 0mL |
硫酸(6mol/L) | 0mL | 2mL | (____)mL | 8mL |
现象 | 无现象 | 溶液呈浅黄色 | 溶液呈黄绿色,生成浅黄绿色气体 | 溶液呈黄绿色, |
①该系列实验的目的_______________________。
②烧杯3取用硫酸的体积应为______________mL。
(5)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色。设计最简单的实验验证Cl2中含有ClO2______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄可用于酿酒。
(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是_______________________________________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是________________________________。
②试管b中盛放的试剂是饱和_________________溶液。
⑧实验开始时,试管b中的导管不伸入液面下的原因是___________________。
④若分离出试管b中生成的乙酸乙酯,需要用到的仪器是____(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近段时间,全国范围内的雾霾天气严重影响了人们的身体健康,环境问题越来越受到人们的重视。处理大气中的污染物,打响“蓝天白云”保卫战是当前的重要课题。请回答下列问题:
(1)汽车尾气中含有较多的NOx和CO,两种气体均会使人体中毒。可以利用如下化学方法将其转化为无毒无害的物质。
已知:N2(g)+O2(g)2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g)2CO2(g) ΔH=-564 kJ·mol-1
请写出把汽车尾气转化为无毒无害的物质的热化学方程式: _________
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)CH3OH(g)。在密闭容器中充有2mol CO和4molH2,在催化剂作用下发生反应生成甲醇,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。则该反应为______反应(填“吸热”或“放热”)。若达到平衡状态A时,容器的体积为2L,则在平衡状态B时容器的体积为_______2L(填“>”、“=”或“<”)。该反应T2温度下,若反应进行到1 min达到平衡状态,用CO的分压变化表示的平均反应速率vp(CO)=_______ kPa·min-1,此时的化学平衡常数Kp=_____(Kp是以分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数))。

(3)工业上可采用CH3OHCO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为______ (填A、B)。
(4)如图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表的一部分,其中A、B、C、D、E代表元素。下列说法错误的是( )

A.元素B、D对应族①处的标识为ⅥA
B.E的含氧酸酸性强于D的含氧酸
C.熔点:D的氧化物<C的氧化物
D.AE3分子中所有原子都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在太空中发现迄今已知最大钻石 直径4000公里,重达100亿万亿万亿克拉。下列关于金刚石的叙述说法正确的是:( )
A.含1molC的金刚石中的共价键为4mol
B.金刚石和石墨是同分异构体
C.C(石墨)![]() C(金刚石) △H=+1.9KJ/mol,说明金刚石比石墨稳定
C(金刚石) △H=+1.9KJ/mol,说明金刚石比石墨稳定
D.石墨转化为金刚石是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )
A | B | C | ||
D | ||||
A.原子半径大小比较为D>C>B>A
B.生成的氢化物分子间均可形成氢键
C.A与C形成的阴离子可能有AC![]() 、A2C
、A2C![]()
D.A、B、C、D的单质常温下均不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,其中X、Y、Z均为短周期元素,它们的位置关系如图所示,已知三种元素的质子数之和为31,写出:
X | ||
Y | Z |
(1)写出X、Y、Z的元素符号:___、___、___。
(2)写出Y元素的离子结构示意图:___。
(3)元素Y和Z的金属性较强的是___(填元素符号)。
(4)Z是大自然赐予人类的宝物。它其中的一个用途是和氧化铁反应制得难熔金属铁,该反应的化学方程式为___,Z表现出的性质是___(氧化性/还原性),反应时可观察到的实验现象有___(填字母)。
A.产生红棕色烟雾 B.发出耀眼的光芒 C.有熔融物生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com