
下列有关同分异构体数目的叙述中,不正确的是( )
| A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B.分子式符合C5H11Cl的化合物有6种 |
| C.已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种 |
D.菲的结构简式为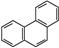 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
B
解析试题分析:A、甲苯苯环上有3种H原子,含3个碳原子的烷基有正丙基、异丙基两种,所以甲苯苯环上的一个氢原子被含3个碳原子的烷基取代有3×2=6产物,故A正确;B、分子式为C5H11Cl的同分异构体有:主链有5个碳原子的:CH3CH2CH2CH2CH2Cl;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;主链有4个碳原子的:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;主链有3个碳原子的:CH2C(CH3)2CH2Cl,所以共有8种情况,故B错误;C、由于苯环含有6个H原子,二氯苯与四氯苯的同分异构体数目相同,若二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种,故C正确;D、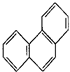 为对称结构,有如图所示的5种H原子
为对称结构,有如图所示的5种H原子 ,所以与硝酸反应,可生成5种一硝基取代物,故D正确;故选B。
,所以与硝酸反应,可生成5种一硝基取代物,故D正确;故选B。
考点:考查同分异构体的书写与判断


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:填空题
如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:
(2)石墨电极(C)的电极反应式为
(3)若在标准状况下,有2. 24 L氧气参加反应,则乙装置中铁电极上生成的气体体积为_ L;丙装置中阴极析出铜的质量为 g
(4)某同学利甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。若用于制漂白液时a为电池_ 极,电解质溶液最好用_ 。若用于制 Fe(OH)2,使用硫酸钠做电解质溶液,阳极选用 作电极。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(8分)请用相关知识回答下列问题:
(1)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,实验过程测得的CO2气体体积随时间变化如右图所示。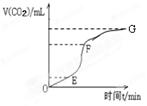
①________段化学反应速率最快,_______段收集的二氧化碳气体最多。
②除加入蒸馏水外,当加入下列物质中的 (填序号)时,则能够减缓上述反应的速率。
A.醋酸钠溶液 B.碳酸钙粉末 C.稀硫酸 D.浓盐酸
(2)原电池是一种能量装置。
①下列在理论上可用来设计原电池的反应是 (填序号)。
A.NaOH +HCl==NaCl+H2O B.2FeCl3+Cu=2FeCl2+CuCl2
C.CuSO4 +2NaOH== Cu(OH)2+NaSO4 D.C2H6O +3O2==3H2O+2CO2
②实验室中用锌片与硫酸反应制取氢气时,向反应溶液中滴加几滴CuSO4溶液,可以发现产生氢气速率明显加快,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16分)某研究小组拟用粗食盐(含Ca2+、Mg2+、SO 等)、粗硅(含C及不与Cl2反应的固体杂质)制取纯硅,设计如下的工艺流程:
等)、粗硅(含C及不与Cl2反应的固体杂质)制取纯硅,设计如下的工艺流程:
试回答下列问题:
(1)工业上一般是利用过量焦炭在高温下还原石英砂来制取粗硅,写出该过程的化学方程式:_______________________________________________________________________。
(2)精制粗盐水所需试剂为①BaC12;②Na2CO3;③HC1;④NaOH,其滴加的先后顺序是下列的________(填下列各项的序号)。
a.①②④③ b.④②①③ c.④①③② d.②④①③
已知, ,假设该粗盐水中
,假设该粗盐水中 的浓度均为0.01 mol·L-1,若向1 L该粗盐水中逐渐滴入一定量Na2CO3溶液,首先出现的沉淀是__________。
的浓度均为0.01 mol·L-1,若向1 L该粗盐水中逐渐滴入一定量Na2CO3溶液,首先出现的沉淀是__________。
(3)已知SiCl4的沸点是57.6℃,CC14的沸点是76.8℃。在反应器I中得到的SiCl4粗品中含有CCl4,从中得到纯净SiCl4可采用的方法是下列各项中的________(填序号)。
a.蒸馏 b.干馏 c.分液 d.过滤
反应器Ⅱ中发生反应的化学方程式为__________________________________________。
(4)下图是用离子交换膜法电解饱和食盐水的示意图,电解槽中阴极产生的气体是_____。产品A的化学式为____________。
若采用无膜电解槽电解饱和食盐水可制取次氯酸钠,试写出该反应的化学方程式__ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、K1O3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下:
①反应I生成铁与碘的化合物,若该化合物中铁元素与碘元素的质量比为21:127,则加入足量碳酸钾时,反应Ⅱ的化学方程式为 。
②操作A包括 ;用冰水洗涤的目的是 。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①烹饪时,含KIO3的食盐常在出锅前加入,其原因是 ,
②若制得1284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水 kg。
③KIO3还可通过下图所示原理进行制备。电解时总反应的离子方程式为 。若忽略溶液体积的变化,则电解结束后阴极区的pH与电解前相比 (选填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知碳碳单键可绕键轴自由旋转,某烃的结构简式如下图所示,下列说法中正确的是
| A.该物质所有原子均可共面 |
| B.分子中至少有10个碳原子处于同一平面上 |
| C.分子中至少有11个碳原子处于同一平面上 |
| D.该烃与苯互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.麦芽糖的水解产物能发生银镜反应 |
| B.四氟乙烯(CF2=CF2)中所有的原子都在同一个平面上 |
C. 在酸性条件下水解产物是 在酸性条件下水解产物是 和 和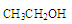 |
| D.淀粉溶液加适量浓硫酸加热一会儿后,滴入银氨溶液无银镜生成,说明淀粉未水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
科学家最近在-100 ℃的低温下合成一种烃X,此分子的模型如下图(图中的连线表示化学键),下列说法正确的是( )
| A.X能使溴的四氯化碳溶液褪色 |
| B.X是一种在常温下能稳定存在的液态烃 |
| C.X分子中在同一平面上的碳原子最多有5个 |
| D.充分燃烧等质量的X和甲烷,X消耗氧气多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com