
| A. | 前者大 | B. | 后者大 | C. | 相等 | D. | 无法确定 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
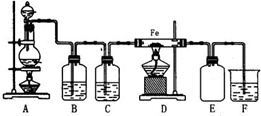 实验室可以用浓盐酸与二氧化锰在加热的条件下反应生成二氯化锰与氯气,纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如图,回答下列问题:
实验室可以用浓盐酸与二氧化锰在加热的条件下反应生成二氯化锰与氯气,纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
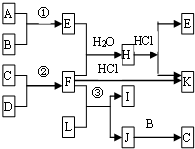 如图是部分短周期元素的单质及其化合物的转化关系图
如图是部分短周期元素的单质及其化合物的转化关系图| 溶液酸碱性 | 离子浓度大小顺序 | |
| 1 | 酸性 | |
| 2 | 中性 | |
| 3 | 碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Br2的CCl4溶液鉴别CH2=CH2和HC≡CH | |
| B. | 用AgNO3溶液鉴别KCl溶液和MgCl2溶液 | |
| C. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| D. | 用酚酞溶液鉴别未知浓度的NaOH溶液和Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据碳酸盐与盐酸反应能放出二氧化碳气体,确定某矿石中是否含碳酸盐 | |
| B. | 根据纤维在火焰上燃烧产生的气味,确定该纤维是否为蛋白质纤维 | |
| C. | 根据加入氯化钡溶液的方法来检验溶液中是否含有硫酸根离子 | |
| D. | 根据氨气能使湿润的红色石蕊试纸变蓝色,可以用于铵根离子的检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
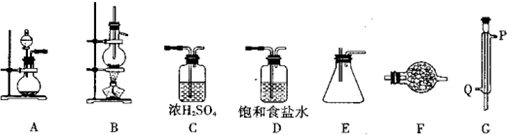
| 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | |
| 四氯化锡 | 2.2 | -33 | 114 |
| 金属锡 | 5.77 | 231 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 间二甲苯的二氯代物有5种 | |
| B. | 二氯甲烷有2种同分异构体 | |
| C. | 丙烯分子中所有的原子有可能在同一平面上 | |
| D. | 用-C4H9取代苯环上的1个氢原子,最多可得4种同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com