
����Ŀ��NaCl��Һ�л���Na2SO4��CaCl2��Һ�͵��۽��壬ѡ���ʵ����Լ��ͷ��������ᴿ��NaCl���塣��Ӧ��ʵ�������ͼ��

��1��д������ʵ������������Լ����Լ��� ���Լ��� ��
��2���ж��Լ����ѹ����ķ����ǣ� ��
��3�������������ð�Ĥ���з����ᴿ�������ٵ�ʵ���������� ����ܡ����ܡ���
����Ĥ��SO42- ����ܡ����ܡ�������Ĥ��
��4���������������� ��
��5��ʵ�������Ƶõ�NaCl��������480mL1.0mol/L��NaCl��Һ����������ƽ�������Ȼ��ƹ���������� �����ƹ����õ��IJ�����������Ͳ���ձ�����ͷ�ι��⣬���� ��
�������²��������Ƶ���ҺŨ����ɵ�Ӱ�죬Ӱ��ƫ�ߵ��� ��
������ˮϴ������ƿ��û�к��
��ת����Һ�����г���©Һ
���ܽ��δ����ȴ��ת�Ƶ�����ƿ
�ܶ���ʱ����
��ҡ�Ⱥ���Һ�潵�ͣ��ټ�����ˮ
���𰸡���1��BaCl2��1������HCl��1����
��2�����ã����ϲ���Һ�еμ������Ȼ�����Һ��û�а�ɫ����������˵���Ȼ�����Һ�ѹ�������2����
��3��������1������ ����1������4�������ᾧ��1����
��5��29.3g��2������500ml����ƿ��1������������2����
��������
�����������1�����岻������Ĥ��������Ϊ��������ȥNa2SO4��CaCl2���ɷֱ����BaCl2��Na2CO3����ȥ�����к��е�Ca2+��SO42-���������ʵķ������������BaCl2��ȥ����������ӣ��ټ������Na2CO3��ȥ���������������Լ���ΪBaCl2��������Ϊ���ˣ�����AΪ���ᱵ���Լ���ΪNa2CO3��������Ϊ���ˣ�����BΪ̼��ƺ�̼�ᱵ���Լ���Ϊ���ᣬ��������ɳ�ȥ������Na2CO3����������ᾧ�ɵõ�NaCl���塣
��2���ж��Լ����ѹ����ķ����Ǿ��ã����ϲ���Һ�еμ������Ȼ�����Һ��û�а�ɫ����������˵���Ȼ�����Һ�ѹ�����
��3�������������ð�Ĥ���з����ᴿ�������ٵ�ʵ���������۲�������Ĥ��SO42-������Ĥ��
��4���������������������ᾧ��
��5��ʵ����û��480mL������ƿ������Ҫ����500mL�Ȼ�����Һ�������Ҫ�Ȼ��Ƶ�������0.5L��1.0mol/L��58.5g��29.25g��������Ҫ��������ƽ�������Ȼ��ƹ����������29.3g�����ƹ����õ��IJ�����������Ͳ���ձ�����ͷ�ι��⣬����500ml����ƿ��������ˮϴ������ƿ��û�к�ɲ�Ӱ��������ת����Һ�����г���©Һ�����ʼ��٣�Ũ��ƫ�ͣ����ܽ��δ����ȴ��ת�Ƶ�����ƿ����������������֪��Һ�������С��Ũ��ƫ�ߣ��ܶ���ʱ������Һ�������С��Ũ��ƫ�ߣ���ҡ�Ⱥ���Һ�潵�ͣ��ټ�����ˮ����Һ��������ӣ�Ũ��ƫС����ѡ�ۢܣ�


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Fe(OH)2¶���ڿ����м����������õIJ���Ϊ( )
A��FeO B��Fe2O3 C��Fe3O4 D��Fe(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A���Ҵ����Ҷ�������������Ϊͬϵ�ͬϵ��֮�䲻����Ϊͬ���칹��
B��������̼�ɱ���Ϊͬ��������
C��C2H5OH��CH3OCH3��Ϊͬ���칹��
D�����ʯ��ʯī��Ϊͬλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ���������ɻ�����Ⱦ����
A������ȼ�ϵ��
B��п�̵��
C�����ӵ��
D��Ǧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л������ʽC16H23Cl3�������в�������������������е�˫����ֵΪ�� ��
A. 5 B. 4 C. 3 D. 2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���������ȷ����
A. ����Ͳ��ȡ25 mL����ˮ B. �÷�Һ©�������Ҵ���ˮ
C. ���ձ��ܽ�FeCl3���� D. ��������ƽ����NaCl����5.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
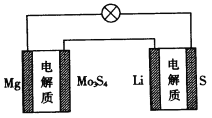
����Ŀ����֪:þ��ص��ܷ�ӦΪxMg+Mo3S4![]() MgxMo3S4������ص��ܷ�ӦΪ2Li+S
MgxMo3S4������ص��ܷ�ӦΪ2Li+S![]() Li2S������˵����ȷ����
Li2S������˵����ȷ����
A��þ��طŵ�ʱ��Mg2+��Ǩ��
B��þ��طŵ�ʱ�����������ĵ缫��ӦΪMo3S4+2xe-= Mo3S42-
C�����������ֵ�صı�������ͬ(����缫��Ӧ�ĵ�λ�����ĵ缫���Ϸų����ܵĴ�С��Ϊ�õ�صı�����)
D��ͼ��Li��������Mo3S4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����ͬŨ�ȵ�NaOH��Һ���ֱ�ζ�100mLŨ�Ⱦ�Ϊ0��1mol��L��1�������ᣨHM��HN��HR����Һ���ζ���������ͼ��ʾ�������жϴ������ �� ��
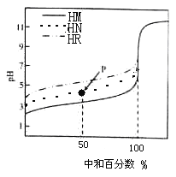
A��������ĵ��볣����ϵ��KHM��KHN��KHR
B��pH=7ʱ��������Һ�У�c��M������c��N������c��R����
C���ζ���P��ʱ����Һ�У�c��Na������ c��N������c��HN����c��H������c��OH����
D�����кͰٷ�����100%ʱ����������Һ��Ϻ� c��HM����c��HN����c��HR��=c(OH��)��c��H����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com