
下列有关热化学方程式的叙述正确的是
A.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq) + CH3COOH(aq) = CH3COONa(aq) + H2O(l);△H = -57.4kJ·mol-1
B.已知C(石墨,s)= C(金刚石,s);△H>0,则石墨比金刚石稳定
C.已知反应2H2(g) + O2(g) = 2H2O(l);△H=-571.6kJ·mol-1,则H2的燃烧热为571.6kJ·mol-1
D.已知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2
科目:高中化学 来源:2014-2015甘肃省张掖市高三第三次诊断考试理综化学试卷(解析版) 题型:实验题
(14分)某实验小组利用下图所示实验装置,使氢气平缓地通过装有金属钙的硬质玻璃管制取氢化钙,并分析产品的成分及纯度。
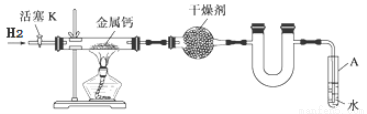
(1)试管A的作用有 ; 。
(2)请将下列制备氢化钙的操作步骤补充完整:
①打开活塞K通入H2;
② ;
③点燃酒精灯,进行反应;
④反应结束后, ;
⑤拆除装置,取出产物。
(3)经分析,产品中只含钙、氢两种元素。取少量产品,小心加入水中,观察到有气泡冒出,滴入一滴酚酞试液,溶液变红。反应的化学方程式可能有CaH2+2H2O=Ca(OH)2+2H2↑、 。
(4)取2.30 g产品溶于蒸馏水,配成500 mL溶液;取25.00 mL该溶液于锥形瓶中,滴入2滴酚酞试液,用0.2500 mol/L 盐酸滴定;三次平行实验,平均消耗盐酸22.00 mL。
①配制溶液所用的玻璃仪器有胶头滴管、烧杯、玻璃棒、量筒、 ;
②判断滴定终点的方法是 ;
③产品中两种成分物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高一上学期期末考试化学试卷(解析版) 题型:选择题
同温同压下,两个等体积的干燥圆底烧瓶中分别充满:①NH3,②NO2,进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为
A.①>② B.①<② C.①=② D.不能确定
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高一上学期期末考试化学试卷(解析版) 题型:选择题
合金是一类用途广泛的金属材料,下列物质中不属于合金的是
A.黄铜 B.黄金 C.青铜 D.钢
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:填空题
(9分)现有浓度均为0.1 mol·L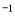 的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H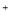 浓度由大到小的顺序是_____(填序号)。
浓度由大到小的顺序是_____(填序号)。
(2)④、⑤、⑥、⑦四种溶液中NH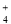 浓度由大到小的顺序是_____(填序号)。
浓度由大到小的顺序是_____(填序号)。
(3)已知t℃时,K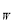 =1×10
=1×10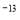 。现在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=_____ 。
。现在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=_____ 。
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
对于反应2X(g) + Y(g)  2Z(g),K表示平衡常数,下列说法正确的是
2Z(g),K表示平衡常数,下列说法正确的是
A.当温度不变时,增大反应物的浓度,使K变小;增大生成物的浓度,使K增大
B.随着反应正向进行,Z的浓度不断增大,X、Y的浓度不断减小,平衡常数不断增大
C.温度发生变化,上述反应的K值也发生变化
D.可逆反应达到平衡时,逆反应便立即停止了
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
一定温度下,可逆反应A2(g)+B2(g) 2AB(g)达到平衡状态的标志是
2AB(g)达到平衡状态的标志是
A.单位时间内生成 n mol A2,同时生成 n mol AB
B.体系内的总压不随时间变化
C.单位时间内生成2n mol AB的同时生成n mol B2
D.单位时间内生成 n mol A2的同时,生成n mol B2
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:选择题
有A,B,C,D四种金属。将A与B用导线连接起来浸入电解质溶液中,B不易腐蚀,将A,D分别投入等浓度的盐酸中,D比A反应剧烈,将铜浸入B的盐溶液中,无明显变化,若将铜浸入C的盐溶液中,有金属C析出。据此判断这四种金属的活动性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C C.D>B>A>C D.B>A>D>C
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市八校高三3月联考理综化学试卷(解析版) 题型:填空题
(14分)
I.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等。按要求回答下列问题:
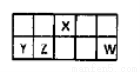
(1)写出X的原子结构示意图 。
(2)列举一个事实说明W非金属性强于Z 。
(3)含Y的某种盐常用作净水剂,其净水原理是 (用离子方程式表示)。
II.运用所学化学原理,解决下列问题:
(4)氰化物多数易溶于水,有剧毒,其中HCN是易挥发的弱酸,已知:Ka(HCN)=6.17x10-10。处理含CN-废水时,用NaOH溶液调节至pH=9时(常温),c(CN-) c(HCN)(填“>”、“<”或“=”)。
(5)已知:
①C(s)+O2(g)===CO2(g);△H =a kJ·mol-1;
②CO2(g) +C(s)===2CO(g);△H =b kJ·mol-1;
③Si(s)+ O2(g)===SiO2(s);△H =c kJ·mol-1。
工业上生产粗硅的热化学方程式为 。
(6)已知:CO(g)+H2O(g)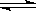 H2(g)+CO2(g)。下表为该反应在不同温度时的平衡常数。
H2(g)+CO2(g)。下表为该反应在不同温度时的平衡常数。

该反应的△H 0(填“>”、“<”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为 。
(7)一种新型氢氧燃料电池工作原理如下图所示。
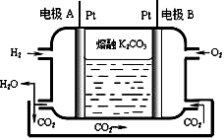
写出电极A的电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com