
| A.反应物的性质 | B.催化剂 |
| C.浓度和压强 | D.温度 |
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③⑤ | B.②⑥ | C.②⑤⑧ | D.②③⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一定浓度稀硫酸与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量K2SO4溶液 |
B.NO+CO2 NO2+CO在密闭容器中进行,压强不变充入N2使体积增大,反应速率不变 |
| C.升高温度时,化学反应速率加快,主要是由于反应物分子的能量增加,活化分子百分数增大,有效 碰撞次数增多,化学反应速率加快 |
| D.催化剂能改变化学反应速率且参与反应,但催化剂在化学反应前后,化学性质和质量都不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH(s) | B.CH3COONa(s) | C.NH4Cl(s) | D.NaHSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
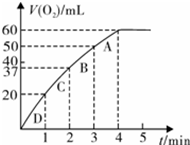
查看答案和解析>>
科目:高中化学 来源:广东省期末题 题型:单选题
查看答案和解析>>
科目:高中化学 来源:广东省期末题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com