
��8�֣�450Kʱ������ʼ�����ͬ���ܱ������г���2mol SO2��1mol O2���䷴Ӧ��2SO2(g)+O2(g) 2SO3(g)��
2SO3(g)��
��H=��96.56kJ/mol����S=��190 J?mol-1?K-1��
�������ڷ�Ӧ�����б���ѹǿ���䣬��������
��������䣬������ά�־��ȣ����������Խ�
����ѧƽ�⡣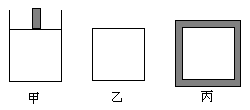
(1)ƽ�ⳣ����K (��) K (��) _ K(��) ���>������<����=������
(2)�ﵽƽ��ʱSO2��ת���ʣ���(��) _ ��(��) _ ��(��)���>������<����=������
(3)�ﵽƽ�������ס����������зֱ�ͨ�������ҵ���Ar���壬 �������Ļ�ѧƽ��________�ƶ����������Ļ�ѧƽ��_________�ƶ���������������� ������
(4)ͨ������ȷ��5000Cʱ����Ӧ ____ ����ܡ� ���ܡ����Է����С�
 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣�450Kʱ������ʼ�����ͬ���ܱ������г���2mol SO2��1mol O2���䷴Ӧ��2SO2(g)+O2(g) 2SO3(g)��
��H=��96.56kJ/mol����S=��190 J•mol-1•K-1��
�������ڷ�Ӧ�����б���ѹǿ���䣬��������
��������䣬������ά�־��ȣ����������Խ�
����ѧƽ�⡣
(1)ƽ�ⳣ����K (��) K (��) _ K(��) ���>������<����=������
(2)�ﵽƽ��ʱSO2��ת���ʣ���(��) _ ��(��) _ ��(��)���>������<����=������
(3)�ﵽƽ�������ס����������зֱ�ͨ�������ҵ���Ar���壬 �������Ļ�ѧƽ��________�ƶ����������Ļ�ѧƽ��_________�ƶ���������������� ������
(4)ͨ������ȷ��5000Cʱ����Ӧ ____ ����ܡ� ���ܡ����Է����С�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���Ĵ�ʡ�ɶ�����УЭ����߶���ѧ������������ѧ�Ծ����������� ���ͣ������
(12��)�ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϡ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
��CH4(g)+H2O(g) CO(g)+3H2(g) �SH1="+206.1" kJ/mol
CO(g)+3H2(g) �SH1="+206.1" kJ/mol
��CH4(g)+CO2(g) 2CO(g)+2H2(g) �SH2="+247.3" kJ/mol
2CO(g)+2H2(g) �SH2="+247.3" kJ/mol
��CO(g)+H2O(g) CO2(g)+ H2(g) �SH3
CO2(g)+ H2(g) �SH3
��ش��������⣺
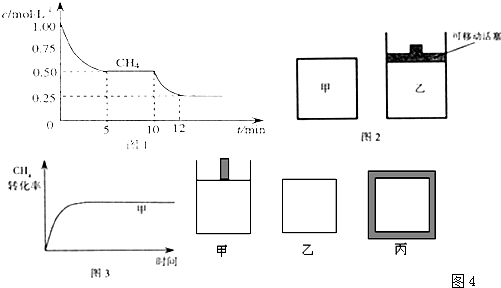
(1)��һ�ܱ������н��з�Ӧ�٣���� �����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ��10minʱ���ı��������������� ��
�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ��10minʱ���ı��������������� ��
(2)��ͼ2��ʾ���ڼס����������зֱ��������ʵ����� ��
�� ��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������
��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䡣��֪�������� ��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������
��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л����������� ��ת������ʱ��仯��ͼ��
��ת������ʱ��仯��ͼ��
(3)��Ӧ����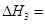 ��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±���
��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±���
��ʱ��Ӧ���������淴Ӧ���ʵĹ�ϵʽ�� (�����)��
a�� (��)
(��) (��) b��
(��) b�� (��)<
(��)< (��) c��
(��) c�� (��)=
(��)= (��) d�����ж�
(��) d�����ж�
��4��800Kʱ������ʼ�����ͬ���ܱ������г���2mol SO2��1mol O2���䷴Ӧ��2SO2(g)+O2(g)  2SO3(g)����H=��96.56 kJ?mol-1���������ڷ�Ӧ�����б���ѹǿ���䣬����������������䣬������ά�־��ȣ����������Խ�����ѧƽ�⡣
2SO3(g)����H=��96.56 kJ?mol-1���������ڷ�Ӧ�����б���ѹǿ���䣬����������������䣬������ά�־��ȣ����������Խ�����ѧƽ�⡣
��1���ﵽƽ��ʱ��ƽ�ⳣ��K (��) K (��) K(��)���>������<����=������
��2���ﵽƽ��ʱSO2��Ũ��C(SO2)(��) C(SO2) (��) C(SO2) (��)���>������<����=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�콭��ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��8�֣�450Kʱ������ʼ�����ͬ���ܱ������г���2mol SO2��1mol O2���䷴Ӧ��2SO2(g)+O2(g)  2SO3(g)��
2SO3(g)��
��H=��96.56kJ/mol����S=��190 J•mol-1•K-1��
�������ڷ�Ӧ�����б���ѹǿ���䣬��������
��������䣬������ά�־��ȣ����������Խ�
����ѧƽ�⡣
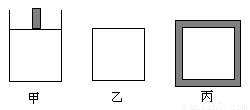
(1)ƽ�ⳣ����K (��) K (��) _ K(��) ���>������<����=������
(2)�ﵽƽ��ʱSO2��ת���ʣ���(��) _ ��(��) _ ��(��)���>������<����=������
(3)�ﵽƽ�������ס����������зֱ�ͨ�������ҵ���Ar���壬 �������Ļ�ѧƽ��________�ƶ����������Ļ�ѧƽ��_________�ƶ���������������� ������
(4)ͨ������ȷ��5000Cʱ����Ӧ ____ ����ܡ� ���ܡ����Է����С�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com