
���� ��1��[RO��OH��2]2+������R�Ļ��ϼ�Ϊ+6�ۣ�n��Na2SO3��=1.2��10-3mol�����������ԭ��Ӧ���������ͻ�ԭ����ʧ������Ŀ���㣻
��2���ٸ���������ԭ��Ӧ�е�ʧ��������Ƚ��ԭ���غ������ƽ��
��HSO3-���л�ԭ�ԣ������ǿ�����ԣ�����HSO3-�ܱ�I2��������SO42-��ͬʱ�ⱻ��ԭ���ɵ����ӣ����ݷ�Ӧ���������д�����ӷ���ʽ��
��� �⣺��1��[RO��OH��2]2+������R�Ļ��ϼ�Ϊ+6�ۣ��軹ԭ��Ļ��ϼ�Ϊx��
n��Na2SO3��=1.2��10-3mol��������������Na2SO4��SԪ�ػ��ϼ�Ϊ+6�ۣ�
��1.2��10-3mol����6-x��=1.2��10-3mol����6-4����x=+4��
�ʴ�Ϊ��D��
��2����NaIO3��Һ�еμ�����NaHSO3��ҺʱHSO3-����������������ӣ�IO3-����ԭ��I2���÷�ӦΪ4NaIO3+10NaHSO3�T2I2+7Na2SO4+3H2SO4+2H2O���÷�Ӧ��ת�Ƶĵ�����Ϊ20e��
�ʴ�Ϊ��4��10��2��7��3��2��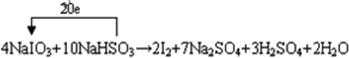 ��
��
�ڻ�ԭ��HSO3-��I-��������I2 ��SO42-��������������������ܱ�������������������ӣ�ͬʱ�ⱻ��ԭ���ɵ����ӣ����������������ܺ͵ⷴӦ�����ӷ�Ӧ����ʽΪ��H2O+I2+HSO3-=2I-+SO42-+3H+��
�ʴ�Ϊ��I2��H2O+I2+HSO3-=2I-+SO42-+3H+��
���� ���⿼��������ԭ��Ӧ�ļ��㣬Ϊ�߿��������ͣ�������ѧ���ķ��������ͼ��������Ŀ��飬ע���Ԫ�ػ��ϼ۵ĽǶȽ����⣬ע����յ����ŷ���ʾ����ת�Ƶķ������ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | sp3��sp2 | B�� | sp3��sp | C�� | sp2��sp | D�� | sp2��sp3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | P4��CH4�Ŀռ乹�ͺͼ��Ƕ���ͬ | |
| B�� | O3��OF2����V��� | |
| C�� | SO3��SeO32-�����幹�Ͷ��������� | |
| D�� | HOCH2CH��OH��CH2OH��CH3CHClCH2CH3�������Է��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʹ��ˮ�е��ηֳ��������� | |
| B�� | ����̫����ʹ��ˮ���� | |
| C�� | ����ˮ���������Ի�ȡ����������ˮ | |
| D�� | ����ˮͨ�����ӽ�����֬���Գ�ȥ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
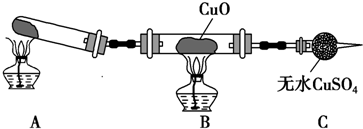
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Al3+��SO42-��HCO3- | B�� | Cu2+��Mg2+��SO42-��NO3- | ||
| C�� | Na+��K+��ClO-��SO42- | D�� | Fe3+��K+��SO42-��I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���� | ���� |
| A | �þƾ��Ƽ���Ħ���Σ�NH4��2Fe��SO4��2•6H2O������������ͨ��װ����ˮ����ͭ�ĸ���� | ������еİ�ɫ��ĩ�ȱ������ɫ�����ֱ������ɫ | �����¶Ƚϵ�ʱĦ���ηֽ����ˮ�������¶��Ը�ʱ�ֽ�������а��� |
| B | ��ij��Һ�еμ�BaCl2��Һ������ϡ�����ữ | ��Һ�в�����ɫ��������ϡ����ܽ� | ԭ��Һ��һ������SO42- |
| C | ��CuSO4��Һ��ͨ��H2S���� | ��Һ����ɫ��ȥ�����ɺ�ɫ���� | ����������Ա�����ǿ |
| D | �����������ͨ������ʻ���ƿ�� | �ʻ���ɫ | ˵����������Ư���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ʒ�����ˮ�У�Na+2H2O�TNa++2OH-+H2�� | |
| B�� | ϡ�������������м��Ӧ��3Fe+8H++2NO3-�T3Fe3++2NO��+4H2O | |
| C�� | SO2ͨ��������ˮ�У�SO2+Cl2+2H2O�TSO42-+2Cl-+4H+ | |
| D�� | ��KAl��SO4��2��Һ�е���Ba��OH��2ǡ��ʹAl3+��ȫ������Ba2++3OH-+Al3++SO42-�TBaSO4��+Al��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t�� | 700 | 800 | 950 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com