

| A、在t1min时,3V正(B)=2V逆(C) |
| B、(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、T℃时,在相同容器中,若由0.3mol?L-1A、0.1 mol?L-1 B和0.4 mol?L-1 C反应,达到平衡后,C的浓度仍为0.4 mol?L-1 |
| D、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
| 0.42 |
| 0.3×0.13 |
| 1600 |
| 3 |
| 0.42 |
| 0.3×0.13 |
| 1600 |
| 3 |


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
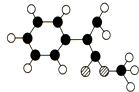
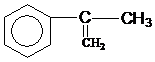 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下: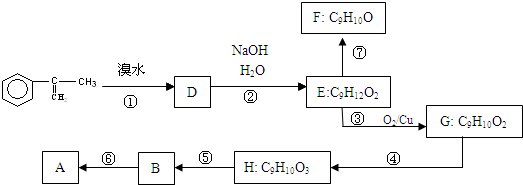
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上利用元素A的单质冶炼金属铁 |
| B、元素C是自然界含量最多的金属元素 |
| C、工业上常用电解法制备元素C、D、E的单质 |
| D、化合物AE与CE有相同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
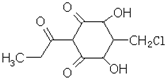
| A、该物质的分子式为:C10H7O5Cl |
| B、1mol该物质在常温下最多可与3mol NaOH反应 |
| C、该物质遇FeCl3溶液不能发生显色反应 |
| D、该物质可发生取代、氧化、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②⑥⑦⑩ | B、①④⑧⑩ |
| C、③⑤⑦⑨ | D、③⑥⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三个烧杯中一定均会发生的离子反应有:2Na+2H2O═2Na++2OH-+H2↑ |
| B、三个烧杯中钠均在液面上剧烈反应,相比而言,X烧杯中的反应平缓些 |
| C、Z烧杯中一定会有沉淀生成,但沉淀不是单质铜 |
| D、三个烧杯中生成氢气体的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
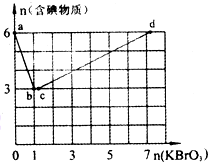 现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加人KBrO3的物质的量的关系如图所示.请回答下列问题:
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加人KBrO3的物质的量的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,48gO3含有的氧原子数为NA个 |
| B、24g金属镁变为镁离子时失去的电子数为NA个 |
| C、在0℃、101kP时,28gN2和CO的混合气体,其体积约为22.4L |
| D、同温同压下,NA个NO与NA个N2和O2的混合气体的体积不相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com